Phản ứng chuyển hóa hydrogen sulfide trong khí thiên nhiên thành sulfur được thực hiện theo sơ đồ phản ứng: H2S + SO2 → S + H2O.
Khối lượng sulfur tối đa tạo ra khi chuyển hóa 1 000 m3 khí thiên nhiên (đkc) (chứa 5 mg H2S/m3) là
-
A.
10,0 g.
-
B.
5,0 g.
-
C.
7,06 g.
-
D.
100,0 g.
Tính khối lượng H2S có trong khí thiên nhiên.
\(\begin{array}{l}2{H_2}S\;\;\; + \;\;\;S{O_2}\;\;\; \to \;\;\;3S\;\;\; + \;\;\;2{H_2}O\\\frac{{1\;000.0,005}}{{34}}.3\; = \;\frac{m}{{32}}.2\; \Leftrightarrow \;m\; = \;7,06\;gam\end{array}\)
Đáp án : C















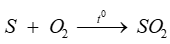 . Sulfur đóng vai trò là
. Sulfur đóng vai trò là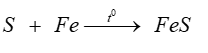





Danh sách bình luận