Phản ứng chuyển hóa hydrogen sulfide trong khí thiên nhiên thành sulfur được thực hiện Theo sơ đồ phản ứng: H2S + SO2 → S + H2O
Khối lượng sulfur tối đa tạo ra khi chuyển hóa 1000m3 khí thiên nhiên (đkc) (chứa 5mgH2S/m3) là
-
A.
10,0g.
-
B.
5,0g.
-
C.
7,06g.
-
D.
100,0g.
Dựa vào phản ứng hydrogen sulfide.
Cứ 1m3 khí thiên nhiên chứa 5mg H2S
=> 1000m3 khí thiên nhiên chứa 5000mg H2S = 5g H2S
nH2S =5:(1.2+32) = 5/34 (mol)
2H2S + SO2 → 3S + 2H2O
5/34 15/68 (mol)
mS = 15/68 .32 \( \approx \) 7,06 (g)
Đáp án : C















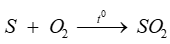 . Sulfur đóng vai trò là
. Sulfur đóng vai trò là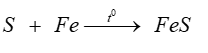





Danh sách bình luận