Cation R3+ có cấu hình electron lớp ngoài cùng là 2p6. Công thức oxide ứng với hóa trị cao nhất, hydroxide tương ứng của R và tính acid – base của chúng là
-
A.
R2O3, R(OH)3 (đều lưỡng tính)
-
B.
RO3 (acidic oxide), H2RO4 (acid)
-
C.
RO2 (acidic oxide), H2RO3 (acid)
-
D.
RO (basic oxide), R(OH)2 (base).
Dựa vào xu hướng biến đổi hợp chất trong bảng tuần hoàn.
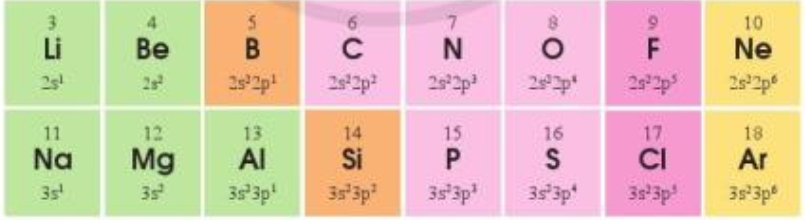
Nguyên tử R đã nhường 3 electron để thành cation R3+ nên R có cấu hình là 1s2 2s22p6 3s2 3p1
Vậy R là nguyên tố aluminium.
A. Đúng
B, C, D sai do hợp chất oxide của R có tính lưỡng tính.
Đáp án A
Đáp án : A




















Danh sách bình luận