Điều chế NH3 từ hỗn hợp gồm N2 và H2 (tỉ lệ mol tương ứng là 1: 3). Tỉ khối của hỗn hợp trước so với hỗn hợp sau phản ứng là 0,6. Hiệu suất phản ứng là?
Đáp án:
Đáp án:
Dựa vào phản ứng tổng hợp NH3.
Giả sử số mol N2 và H2 ban đầu lần lượt là 1 và 3 mol
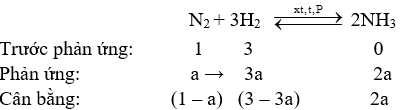
Vì tỉ khối của hỗn hợp trước phản ứng so với hỗn hợp sau phản ứng là 0,6 nên ta có:
\(\begin{array}{l}\frac{{{M_T}}}{{{M_S}}} = 0,6 \to {M_T} = 0,6.{M_S} \to \frac{{{m_{{N_2}}} + {m_{{H_2}}}}}{{{n_{{N_2}}} + {n_{{H_2}}}}} = 0,6.\frac{{{m_{{N_2}}} + {m_{{H_2}}} + {m_{NH3}}}}{{{n_{{N_2}}} + {n_{{H_2}}} + {n_{N{H_3}}}}}\\ \to \frac{{1.28 + 3.2}}{{1 + 3}} = 0,6.\frac{{(1 - a).28 + (3 - 3{\rm{a}}).2 + 2{\rm{a}}.17}}{{(1 - a) + (3 - 3{\rm{a}}) + 2{\rm{a}}}} \to a = 0,8\end{array}\)
Hiệu suất phản ứng: \(\frac{{{n_{{H_2}p/u}}}}{{{n_{{H_2}}}}}.100 = \frac{{3 - 3.0,8}}{3}.100 = 20\% \)



















Danh sách bình luận