Bột đá vôi có thể được sử dụng để xử lí khí thải chứa sulfur dioxide từ các nhà máy điện đốt than và dầu mỏ. Phương trình hóa học của phản ứng là:
CaCO3(s) + SO2 (g) → CaSO3(g) + CO2(g)
a. Phản ứng trên là phản ứng oxi hóa – khử.
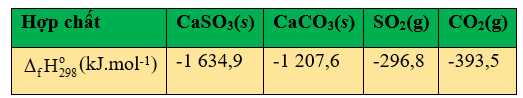
b. Cho giá trị enthalpy chuẩn của các hợp chất trong bảng sau đây. Từ đó xác định được phản ứng trên là phản ứng tỏa nhiệt.
c. Trong phản ứng trên, để phản ứng xảy ra nhanh thì đá vôi phải ở dạng viên lớn.
d. Calcium sulfite (CaSO3) thường được chuyển hóa thành thạch cao có công thức CaSO4.2H2O. Phản ứng ứng chuyển hóa này là một phản ứng oxi hóa - khử.
a. Phản ứng trên là phản ứng oxi hóa – khử.
b. Cho giá trị enthalpy chuẩn của các hợp chất trong bảng sau đây. Từ đó xác định được phản ứng trên là phản ứng tỏa nhiệt.

c. Trong phản ứng trên, để phản ứng xảy ra nhanh thì đá vôi phải ở dạng viên lớn.
d. Calcium sulfite (CaSO3) thường được chuyển hóa thành thạch cao có công thức CaSO4.2H2O. Phản ứng ứng chuyển hóa này là một phản ứng oxi hóa - khử.
Dựa vào công thức tính enthalpy của phản ứng.
a. đúng, vì có sự thay đổi số oxi hóa của C và S.
b. đúng
\(\begin{array}{l}{\Delta _r}H_{298}^o = {\Delta _f}H_{298}^o(CaS{O_3}) + {\Delta _f}H_{298}^o(C{O_2}) - {\Delta _f}H_{298}^o(CaC{O_3}) - {\Delta _f}H_{298}^o(S{O_2})\\ = - 1634,9 + ( - 393,5) - ( - 1207,6) - ( - 296,8) = - 524kJ\end{array}\)
c. sai, cần nghiền nhỏ đá vôi để tăng diện tích bề mặt tiếp xúc.
d. đúng



















Danh sách bình luận