Cho cân bằng sau:

Thực hiện phản ứng trên trong bình kín có dung tích không đổi, tại nhiệt độ T. Ban đầu lấy số mol H2 gấp đôi số mol I2. Tại thời điểm cân bằng, số mol HI gấp đôi số mol I2. Hằng số cân bằng KC của phản ứng trên là
-
A.
4,00
-
B.
1,33
-
C.
1,67
-
D.
2,67
Dựa vào công thức tính hằng số cân bằng Kc.
Gọi số mol I2 ban đầu là 1 mol; n H2 = 2 mol
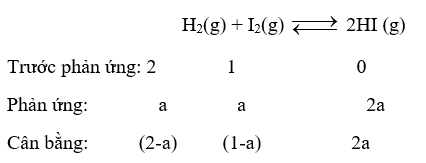
Vì tại cân bằng: n HI = 2.n I2 \( \to \) 2a = 2.(1-a) → a = 0,5 mol
Kc = \(\frac{{{{{\rm{[}}HI]}^2}}}{{{\rm{[}}{H_2}{\rm{]}}.{\rm{[}}{I_2}{\rm{]}}}} = \frac{{{{(2.0,5)}^2}}}{{(2 - 0,5).(1 - 0,5)}} = \frac{4}{3}\)
Đáp án B
Đáp án : B



















Danh sách bình luận