Những trường hợp nào sau đây có xảy ra ăn mòn điện hoá? Giải thích.
a) Cho một mẩu sodium vào dung dịch copper(II) sulfate.
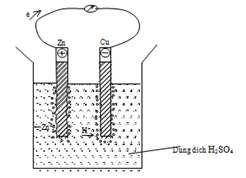
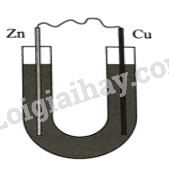
b) Nhúng một thanh kẽm vào dung dịch silver nitrate.
c) Nhúng một thanh sắt vào dung dịch iron(III) chloride.
d) Cho nước vào hỗn hợp bột magnesium, sắt và muối ăn.
e) Trộn bột \({\rm{Zn}}\) vào bột CuSO4.
Dựa vào sự ăn mòn kim loại.
a) Không có ăn mòn điện hoá.
b) \({\rm{Zn(s) + 2A}}{{\rm{g}}^{\rm{ + }}}{\rm{(aq)}} \to {\rm{Z}}{{\rm{n}}^{{\rm{2 + }}}}{\rm{(aq) + 2Ag(s)}}\)
Anode: Zn \( \to \)Zn2+ + 2e
Cathode: Ag+ +1e \( \to \) Ag
c) \({\rm{Fe(s) + 2F}}{{\rm{e}}^{{\rm{3 + }}}}{\rm{(aq)}} \to {\rm{3F}}{{\rm{e}}^{{\rm{2 + }}}}{\rm{(aq)}}\), không có cặp hai kim loại hay kim loại phi kim nên không xảy ra ăn mòn điện hoá.
d) Mg đóng vai trò là anode, Fe đóng vai trò là cathode, nước hoà tan NaCl tạo thành dung dịch chất điện li, nên xảy ra ăn mòn điện hoá.
e) Ở dạng rắn, hai chất không phản ứng với nhau, không đủ điều kiện xảy ra ăn mòn điện hoá.



















Danh sách bình luận