Trong công nghiệp, nhôm được sản xuất bằng phương pháp điện phân nóng chảy aluminium oxide với các điện cực làm bằng than chì, sử dụng cryolite (Na3AlF6) nóng chảy làm xúc tác.
a) Viết các phương trình hóa học của phản ứng có thể xảy ra trong quá trình sản xuất nhôm.
b) Tính lượng quặng bauxite (chứa 80% Al2O3) và lượng than chì cần dùng để sản xuất 2,7 tấn nhôm. Giả sử hiệu suất chế biến quặng và quá trình điện phân là 100%; khí thoát ra tại anode gồm 10% O2; 10% CO và 80% CO2 về thể tích.
Dựa vào các phương pháp tách chất.
a) Phương trình hóa học của các phản ứng có thể xảy ra trong quá trình sản xuất nhôm:
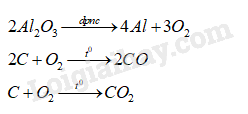
b) Theo đề, ta có:
\({n_{Al}} = \frac{{2,{{7.10}^3}}}{{27}} = 100\,(kmol)\)
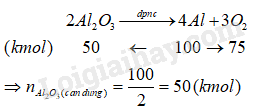
Lượng Al2O3 cần dùng để sản xuất nhôm là
\({m_{A{l_2}{O_3}}} = 50.1022 = 5100\,(kg)\, = \,5,1\,\)(tấn)
Do quặng chứa 80% Al2O3, do đó khối lượng quặng cần dùng là
\(m = \frac{{5,1.100}}{{80}} = 6,375\,\)(tấn)
Tương tự, ta có số mol oxygen sinh ra là
\({n_{{O_2}}} = \frac{{3.100}}{4} = 75\,(kmol)\)
Gọi x là số mol oxygen phản ứng với C tạo sản phẩm CO, y là số mol oxygen phản ứng với C tạo sản phẩm CO2. Ta có:
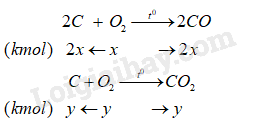
Trong hỗn hợp khí thoát ra chứa 2x (kmol) CO (10%); y kmol CO2 (80%) và z mol O2 dư (10%).
Ta có:
\(\left\{ \begin{array}{l}x + y + z = 75\\z = 2x\\y = 8z = 16x\end{array} \right. \Rightarrow \left\{ \begin{array}{l}2x = 7,895\\z = 7,895\\y = 63,158\end{array} \right.\)
Tương ứng là 7,895 kmol CO; 63,158 kmol CO2 và 7,895 kmol O2.
\( \to \)nC (phản ứng) = 2x + y = 71,053 (kmol)
\( \to \)mC (phản ứng) =71,053. 12 = 852,636 (kg).



















Danh sách bình luận