Cho kí hiệu nguyên tố: \(_{24}^{52}X\)
Nguyên tử X có tổng các hạt mang điện nhiều hơn số hạt không mang điện là 20.
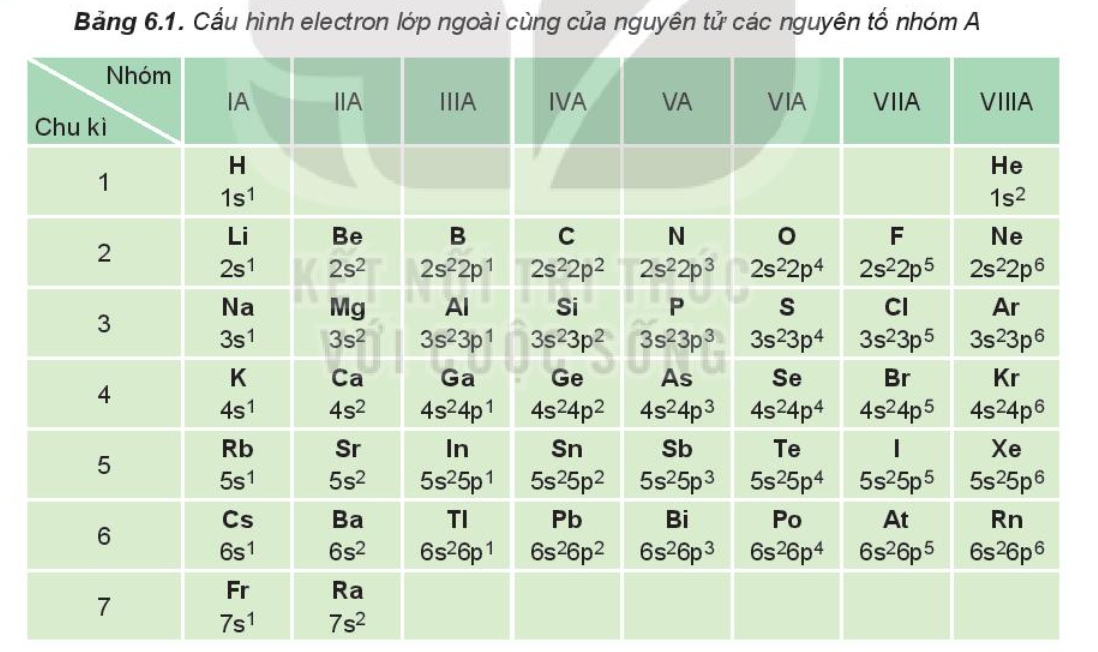
Nguyên tử X có 4 lớp electron.
Cấu hình electron của nguyên tử X là [Ar]3d44s2
X là kim loại.
Nguyên tử X có tổng các hạt mang điện nhiều hơn số hạt không mang điện là 20.
Nguyên tử X có 4 lớp electron.
Cấu hình electron của nguyên tử X là [Ar]3d44s2
X là kim loại.
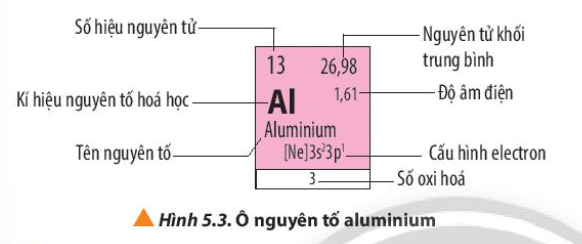
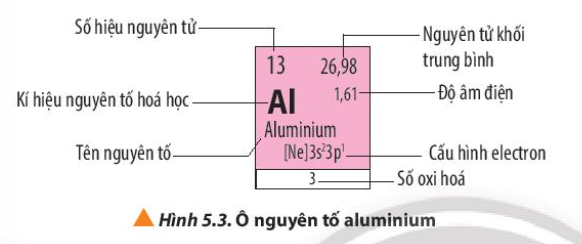
Dựa vào kí hiệu nguyên tố hóa học.
a. đúng, tổng số hạt mang điện của X là 48, hạt không mang điện là 28.
b. đúng
c. sai, cấu hình electron của X là [Ar]3d54s1
d. đúng





















Danh sách bình luận