Cho m gam bột Fe vào dung dịch HNO3 lấy dư, ta được hỗn hợp gồm hai khí NO2 và NO có VX = 9,916 lít (đkc) và tỉ khối đối với O2 bằng 1,3125. Khối lượng của Fe đã dùng là bao nhiêu ? (Fe = 56, N = 14, O =16)
Dựa vào tính chất hóa học của nitric acid.
MX = 1,3125.32 = 42
n X = 9,916 : 24,79 = 0,4 mol
Gọi số mol NO2 và NO lần lượt là a và b mol
Ta có: \(\left\{ \begin{array}{l}a + b = 0,4\\46{\rm{a}} + 30b = 42.0,4\end{array} \right. \to \left\{ \begin{array}{l}a = 0,3\\b = 0,1\end{array} \right.\)
Bảo toàn electron ta có:
Fe0 \( \to \)Fe+3 + 3e N+5 +1e\( \to \)N+4
N+5 + 3e\( \to \)N+2
Áp dụng ĐLBTe \( \to \) nFe.3 = 1.nNO2 + 3.nNO \( \to \) nFe = 0,2 mol \( \to \) mFe = 11,2 gam.














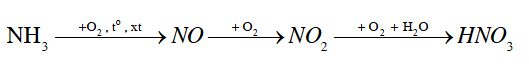
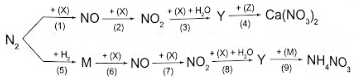
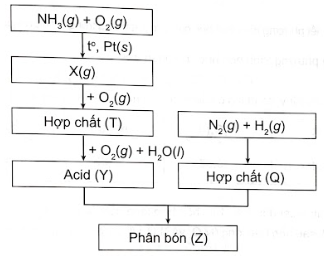
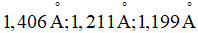 Công thức (A) hay (B) có thể thỏa mãn các số liệu đã cho? Giải thích.
Công thức (A) hay (B) có thể thỏa mãn các số liệu đã cho? Giải thích.




Danh sách bình luận