Thuỷ ngân là kim loại nặng rất độc. Việc con người tiếp xúc với thuỷ ngân trong thời gian dài dẫn đến run rẩy, mất khả năng điều hoà vận động, thay đổi tính cách, mất trí nhớ, mất ngủ, mệt mỏi, đau đầu, giảm cân, căng thẳng tâm lí và viêm lợi. Các triệu chứng này xảy ra khi một người tiếp xúc với nồng độ thuỷ ngân trong không khí trên 50 µg/m3 . Thuỷ ngân độc hơn khi ở thể hơi vì dễ dàng hấp thụ vào cơ thể qua nhiều con đường như đường hô hấp, đường tiêu hoá, qua da, ... Trong trường hợp thuỷ ngân rơi vãi, cần xử lí như thế nào? Liên hệ với tình huống xử lí an toàn khi vô tình làm vỡ nhiệt kế thuỷ ngân trong phòng thí nghiệm.
Thủy ngân phản ứng với lưu huỳnh ở nhiệt độ thường.
Khi thu hồi thuỷ ngân rơi vãi người ta thường sử dụng bột lưu huỳnh rắc lên những chỗ có thuỷ ngân, vì lưu huỳnh có thể tác dụng với thuỷ ngân tạo thành HgS dạng rắn và không bay hơi:
Khi vô tình làm vỡ nhiệt kế thuỷ ngân trong phòng thí nghiệm, cần rắc ngay bột lưu huỳnh bao phủ tất cả các mảnh vỡ. Sau đó dùng chổi quét sạch, gói vào giấy và cho vào thùng rác.















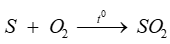 . Sulfur đóng vai trò là
. Sulfur đóng vai trò là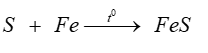





Danh sách bình luận