Cho cân bằng hóa học sau:
CO( g ) + H 2 O( g ) ⇌ CO 2 ( g ) + H 2 ( g )
Ở 700 o C, cân bằng hằng số K C = 8,3. Cho 1 mol khí CO và 1 mol hơi nước vào bình kín, dung tích 10 lít và giữ ở 700 o C. Tính nồng độ các chất ở trạng thái cân bằng.
\(\left( {{\rm{CO}}} \right) = \frac{1}{{10}} = 0,{\rm{1 M}}\); \(\left( {{{\rm{H}___2}{\rm{O}}} \right) = \frac{1}{{10}} = 0,{\rm{1 M}}\ )
CO( g ) + H 2 O( g ) ⇌ CO 2 ( g ) + H 2 ( g )
Ban đầu: 0,1 0,1 0 0 M
Phản ứng: x x x x M
Cân bằng: (0,1 – x) (0,1 – x) x x M
Thay đổi công thức số:
\({{\rm{K}__{\rm{C}}} = \frac{{\left( {{\rm{C}}{{\rm{O}__{\rm{2} }}} \right)\left( {{{\rm{H}__{\rm{2}}}} \right)}}{{\left( {{\rm{CO}}} \right) \left( {{{\rm{H}__{\rm{2}}}{\rm{O}}} \right)}}\)
Ta có: [CO] =\(\frac{1}{{10}} = 0,1M\); [H2O] = \(\frac{1}{{10}} = 0,1M\)
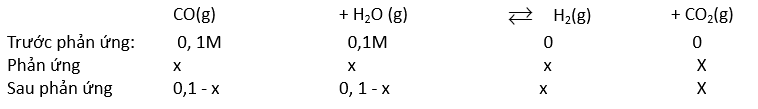
\(\begin{array}{l}{K_C} = \frac{{{\rm{[}}{H_2}]{\rm{[}}C{O_2}]}}{{{\rm{[}}CO]{\rm{[}}{H_2}O]}} = \frac{{x.x}}{{(0,1 - x).(0,1 - x)}} = 8,3\\x = 0,074M\\{\rm{[}}CO] = {\rm{[}}{H_2}O] = 0,1 - 0,074 = 0,026M\\{\rm{[}}{H_2}] = {\rm{[}}C{O_2}] = 0,074M\end{array}\)



















Danh sách bình luận