Dữ liệu thí nghiệm của phản ứng: SO2Cl2(g) → SO2(g) + Cl2(g) được trình bày ở bảng sau: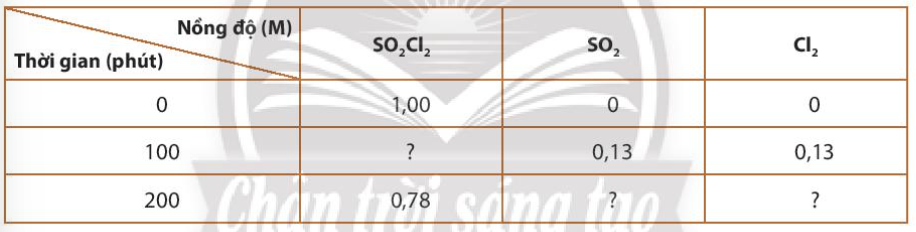
a) Tính tốc độ trung bình của phản ứng theo SO2Cl2 trong thời gian 100 phút.
b) Sau 100 phút, nồng độ của SO2Cl2 còn lại là bao nhiêu
c) Sau 200 phút, nồng độ của SO2 và Cl2 thu được là bao nhiêu?
Áp dụng công thức: \(\mathop v\limits^\_ = - \frac{1}{a}\frac{{\Delta {C_A}}}{{\Delta t}} = - \frac{1}{b}\frac{{\Delta {C_B}}}{{\Delta t}} = \frac{1}{c}\frac{{\Delta {C_C}}}{{\Delta t}} = \frac{1}{d}\frac{{\Delta {C_D}}}{{\Delta t}}\)
a) Trong 100 phút, chất tạo thành từ 0M tăng lên 0,13M
=> ∆C = 0,13M
\(\mathop v\limits^\_ = \frac{1}{1}\frac{{\Delta {C_{S{O_2}C{l_{_2}}}}}}{{\Delta t}} = \frac{1}{1}\frac{{0,13}}{{100}} = 1,{3.10^{ - 3}}(M/phut)\)
b) Ta có: -∆CSO2Cl2 = 0,13M = 1,00 – C2
=> C2 = 0,87M
c) Sau 200 phút
-∆CSO2Cl2 = C1 – C2 = 1,00 – 0,78 = 0,22M
=> Sau 200 phút, nồng độ của SO2 và Cl2 = 0,22M



















Danh sách bình luận