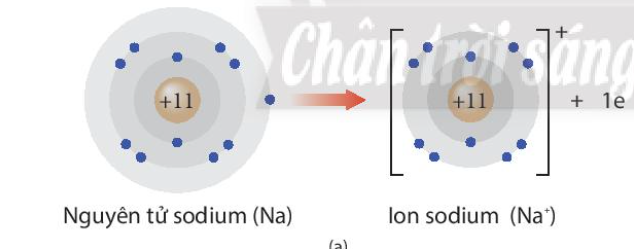
Giải thích sự hình thành ion Na+ và ion F-
- Na là kim loại, nguyên tử dễ nhường electron
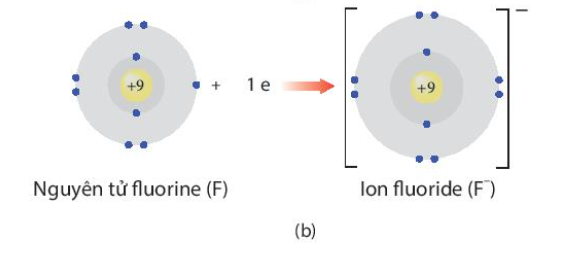
- F là phi kim, nguyên tử dễ nhận electron
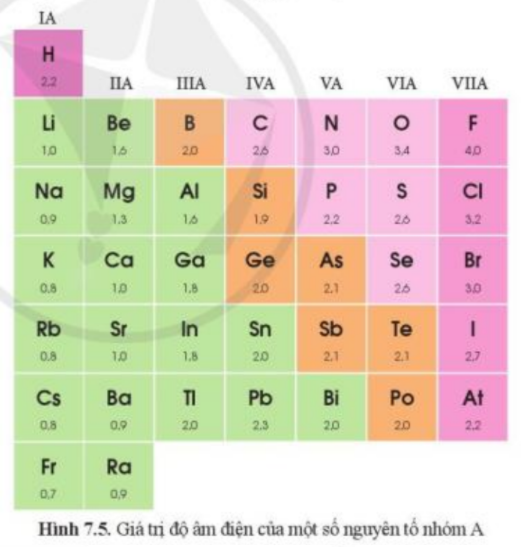
- Na là kim loại nhóm IA => Có 1 electron ở lớp ngoài cùng => Khi tham gia liên kết dễ dàng nhường đi 1 electron để đạt cấu hình electron bền vững khí hiếm, tạo thành Na+
- F là phi kim nhóm VIIA => Có 7 electron ở lớp ngoài cùng => Khi tham gia liên kết dễ dàng nhận thêm 1 electron để đạt cấu hình electron bền vững của khí hiếm, tạo thành F-






















Danh sách bình luận