Cân bằng sau chuyển dịch theo chiều nào khi tăng nhiệt độ?
2SO2 (g) + O2 (g) ⇌ 2SO3 (g) \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}{\rm{ = - 197}}{\rm{,8 kJ}}\]
Khi một phản ứng thuận nghịch ở trạng thái cân bằng, nếu thay đổi nhiệt độ thì cân bằng cũ sẽ bị phá vỡ, cân bằng mới được hình thành theo chiều làm giảm sự thay đổi nhiệt độ đó. Ta gọi đây là sự chuyển dịch cân bằng (từ cân bằng cũ sang cân bằng mới).
Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu tác động từ bên ngoài như biến đổi nhiệt độ, nồng độ hay áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
Theo chiều thuận: \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\]= -197,8 kJ < 0 → Chiều thuận tỏa nhiệt.
Theo chiều nghịch: \[{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\]= 197,8 kJ > 0 → Chiều nghịch thu nhiệt.
Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều làm giảm tác động của việc tăng nhiệt độ, nghĩa là cân bằng chuyển dịch theo chiều thu nhiệt (chiều nghịch).














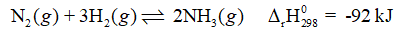 dịch theo chiều nào (có giải thích) khi:
dịch theo chiều nào (có giải thích) khi:




Danh sách bình luận