Xét các hệ cân bằng sau trong một bình kín:
a) \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)= 131 kJ
b) \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)= -41 kJ
Các cân bằng trên dịch chuyển theo chiều nào khi thay đổi một trong các điều kiện sau?
(1) Tăng nhiệt độ.
(2) Thêm lượng hơi nước vào hệ.
(3) Thêm khí H2, vào hệ.
(4) Tăng áp suất chung bằng cách nén cho thể tích của hệ giảm xuống.
(5) Dùng chất xúc tác.
Nguyên lí Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động từ bên ngoài như biến đổi nồng độ, áp suất, nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động đó.
Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều phản ứng thu nhiệt, nghĩa là chiều làm giảm tác động của việc tăng nhiệt độ. Ngược lại, khi giảm nhiệt độ, cân bằng chuyển dịch theo chiều phản ứng toả nhiệt, chiều làm giảm tác động của việc giảm nhiệt độ.
Khi tăng hoặc giảm nồng độ một chất trong cân bằng thì cân bằng chuyển dịch theo chiều làm giảm tác động của việc tăng hoặc giảm nồng độ của chất đó, nghĩa là cân bằng sẽ chuyển dịch tương ứng theo chiều làm giảm hoặc tăng nồng độ của chất đó.
Khi hệ đang ở trạng thái cân bằng, nếu tăng hoặc giảm áp suất của hệ, cân bằng chuyển dịch theo chiều làm giảm hoặc tăng áp suất của hệ.
Chất xúc tác không làm thay đổi nồng độ các chất trong hệ cân bằng và cũng không làm thay đổi hằng số cân bằng nên không làm chuyển dịch cân bằng.
a)
|
\({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)= 131 kJ |
|
|
Tác động |
Cân bằng chuyển dịch |
|
Tăng nhiệt độ |
Cân bằng chuyển dịch theo chiều thuận (vì tăng nhiệt độ, cân bằng chuyển dịch theo chiều làm giảm nhiệt độ của hệ - chiều thu nhiệt, phản ứng theo chiều thuận là phản ứng thu nhiệt) |
|
Thêm lượng hơi nước vào hệ |
Cân bằng chuyển dịch theo chiều thuận (vì khi thêm nước tức là tăng nồng độ chất phản ứng, cân bằng chuyển dịch theo chiều làm giảm nồng độ chất phản ứng là chiều thuận) |
|
Thêm khí H2, vào hệ |
Cân bằng chuyển dịch theo chiều nghịch (vì khi thêm H2 tức là tăng nồng độ sản phẩm, cân bằng chuyển dịch theo chiều làm giảm nồng độ sản phẩm là chiều nghịch) |
|
Tăng áp suất chung bằng cách nén cho thể tích của hệ giảm xuống |
Cân bằng chuyển dịch theo chiều nghịch (vì số mol khí vế trái là 1, tổng số mol khí vế phải là 2 mol, khi tăng áp suất, cân bằng chuyển dịch theo chiều làm giảm áp suất – giảm số mol khí của hệ là chiều nghịch) |
|
Dùng chất xúc tác |
Không làm chuyển dịch cân bằng. |
b)
|
\({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)= -41 kJ |
|
|
Tác động |
Cân bằng chuyển dịch |
|
Tăng nhiệt độ |
Cân bằng chuyển dịch theo chiều nghịch (vì tăng nhiệt độ, cân bằng chuyển dịch theo chiều làm giảm nhiệt độ của hệ - chiều thu nhiệt, phản ứng theo chiều nghịch là phản ứng thu nhiệt) |
|
Thêm lượng hơi nước vào hệ |
Cân bằng chuyển dịch theo chiều thuận (vì khi thêm nước tức là tăng nồng độ chất phản ứng, cân bằng chuyển dịch theo chiều làm giảm nồng độ chất phản ứng là chiều thuận) |
|
Thêm khí H2, vào hệ |
Cân bằng chuyển dịch theo chiều nghịch (vì khi thêm H2 tức là tăng nồng độ sản phẩm, cân bằng chuyển dịch theo chiều làm giảm nồng độ sản phẩm là chiều nghịch) |
|
Tăng áp suất chung bằng cách nén cho thể tích của hệ giảm xuống |
Cân bằng không chuyển dịch (vì tổng số mol khí ở hai vế giống nhau (2 mol) nên áp suất không ảnh hưởng) |
|
Dùng chất xúc tác |
Không làm chuyển dịch cân bằng. |














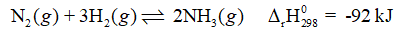 dịch theo chiều nào (có giải thích) khi:
dịch theo chiều nào (có giải thích) khi:




Danh sách bình luận