Viết cấu hình electron của các ion K+, Mg2+, F-, S2-. Mỗi cấu hình đó giống với cấu hình electron của nguyên tử khí hiếm nào?
K (e =19) à K+( e = 18)
Mg (e =12) à Mg2+(e =10)
F (e=9) à F- (e=10)
S (e =16) à S2- (e = 18)
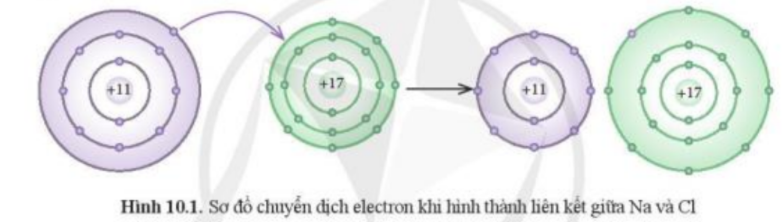
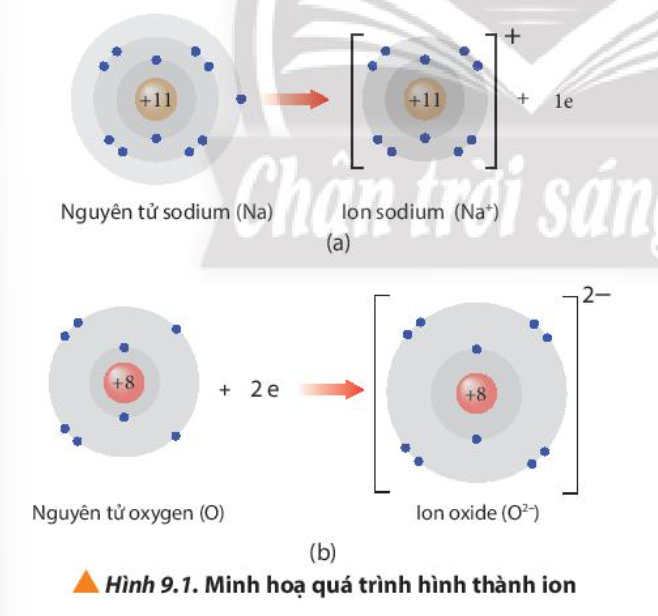
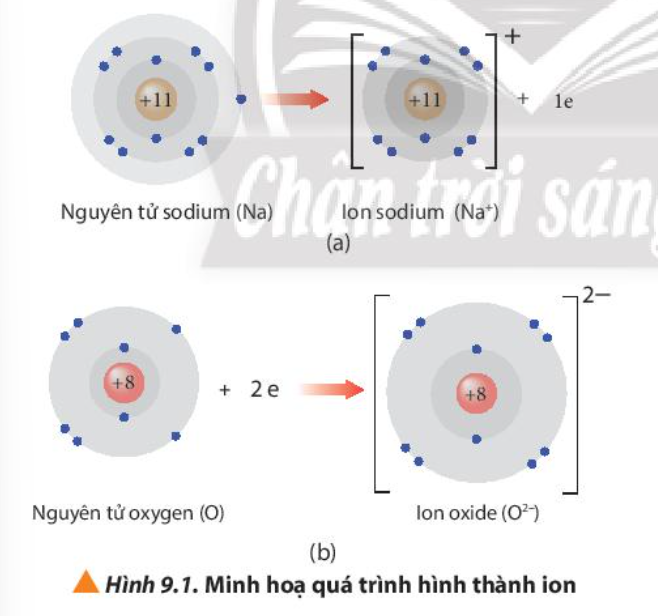
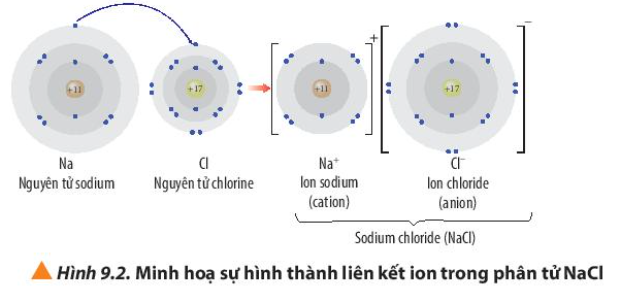
Các ion thường có cấu hình electron bền vững của nguyên tử khí hiếm gần nhất với nguyên tố tạo thành ion đó trong bảng tuần hoàn.
K+( e = 18): 1s22s22p63s23p6 => Cấu hình electron giống nguyên tử Ar.
Mg2+(e =10): 1s22s22p6 => Cấu hình electron giống nguyên tử Ne.
F- (e =10): 1s22s22p6 => Cấu hình electron giống nguyên tử Ne.
S2- (e = 18): 1s22s22p63s23p6 => Cấu hình electron giống nguyên tử Ar.




















Danh sách bình luận