
Phản ứng đốt cháy quặng tạo ra khí SO2.
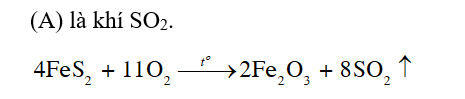


Phản ứng đốt cháy quặng tạo ra khí SO2.
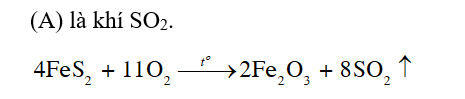

Các bài tập cùng chuyên đề
Bài 1 :
Kể tên một ứng dụng thực tiễn của quặng pyrite, thạch cao, sulfuric acid mà em biết.
Bài 2 :
Sưu tầm thông tin và trình bày về ứng dụng của một hợp chất có chứa nguyên tố sulfur trong thực tiễn.
Bài 3 :
1. Sulfur dioxide là oxide acid (acidic oxide). Viết phương trình hoá học minh họa.
2. Dựa vào số oxi hoá của sulfur trong hợp chất sulfur dioxide, hãy dự đoán tính oxi hoá, tính khử của sulfur dioxide.
Bài 4 :
Hãy xác định sự thay đổi số oxi hóa của nguyên tử các nguyên tố và vai trò của sulfur dioxide trong phản ứng của sulfur dioxide với hydrogen sulfide và nitrogen dioxide.
Bài 5 :
a) Trình bày ứng dụng của sulfur dioxide. Giải thích.
b) Kể tên một số nguồn phát thải sulfur dioxide vào khí quyển. Em hãy đề xuất một số biện pháp nhằm cắt giảm sự phát thải đó.
Bài 6 :
Xác định tính oxi hóa, tính khử của mỗi chất trong các phản ứng hóa học (1) và (2).
\[\begin{array}{l}{\rm{S}}{{\rm{O}}_{\rm{2}}}{\rm{ + N}}{{\rm{O}}_{\rm{2}}} \to {\rm{S}}{{\rm{O}}_{\rm{3}}}{\rm{ + NO (1)}}\\{\rm{S}}{{\rm{O}}_{\rm{2}}}{\rm{ + 2}}{{\rm{H}}_{\rm{2}}}{\rm{S}} \to 3{\rm{S + 2}}{{\rm{H}}_2}{\rm{O (2)}}\end{array}\]
Bài 7 :
Nêu một số nguồn phát thải sulfur dioxide và tác hại của loại khí này.
Bài 8 :
Giải thích sự hình thành mưa acid từ sulfur dioxide.
Bài 9 :
Em hãy tìm hiểu và đề xuất một số giải pháp phù hợp với lứa tuổi học sinh giúp giảm thiểu lượng sulfur dioxide thải vào không khí.
Bài 10 :
Số oxi hoá của sulfur trong phân tử SO2 là
A. +4 B. -2
C. +6 D. 0
Bài 11 :
Khí SO2 do các nhà máy thải ra là nguyên nhân chính trong việc gây ô nhiễm môi trường. Theo quy chuẩn kĩ thuật quốc gia về chất lượng không khí xung quanh (QCVN 05:2013/BTNMT) thì nếu lượng SO2 vượt quá 350 µg/m3 không khí đo trong 1 giờ ở một thành phố thì coi như không khí bị ô nhiễm. Nếu người ta lấy 50 lít không khí trong 1 giờ ở một thành phố và phân tích thấy có 0,012 mg SO2 thì không khí ở đó có bị ô nhiễm không?
Bài 12 :
Sulfur dioxide thuộc loại oxide acid. Hãy cho biết sulfur dioxide có phản ứng được với calcium hydroxide, calcium oxide không. Viết phương trình hoá học của phản ứng xảy ra (nếu có).
Bài 13 :
Hãy đề nghị công thức Lewis của SO2.
Bài 14 :
Nguyên tử sulfur thể hiện nhiều số oxi hoá khác nhau trong các hợp chất, như -2, +4, +6. Hãy giải thích vì sao SO2 có cả tính khử và tính oxi hoá.
Bài 15 :
Hãy giải thích cơ sở hóa học của một số biện pháp giảm thải lượng sulfur dioxide vào không khí.
Bài 16 :
Vì sao nói hydrogen cũng như ethanol là nhiên liệu thân thiện với môi trường (nhiên liệu xanh)?
Bài 17 :
Cả sulfur và sulfur dioxide đều là những chất vừa có tính oxi hoá, vừa có tính khử. Hãy viết phương trình hoá học minh hoạ.
Bài 18 :
Quá trình hoà tan bột đồng bởi dung dịch sulfuric acid đặc sẽ sinh ra khí sulfur dioxide. Nhằm hạn chế phát tán sulfur dioxide ra môi trường, các hoá chất nào sau đây có thể được dùng để hấp thụ khí này: dung dịch sodium hydroxide, dung dịch nước vôi trong, dung dịch hydrochloric acid? Giải thích.
Bài 19 :
Tại một số nhà máy, người ta dùng calcium oxide (vôi sống) hoặc calcium hydroxide (vôi tôi) để hấp thụ sulfur dioxide trong khí thải.
a) Viết phương trình hoá học của các phản ứng trên.
b) Ở mỗi phản ứng, sulfur dioxide thể hiện tính chất gì?
Bài 20 :
Bột đá vôi có thể được sử dụng để xử lí khí thải chứa sulfur dioxide từ các nhà máy điện đốt than và dầu mỏ. Phương trình hoá học của phản ứng là:
CaCO3(s) + SO2(g) → CaSO3(s) + CO2(g)
a) Vì sao phản ứng trên được gọi là phản ứng khử sulfur trong khí thải?
b) Tính giá trị biến thiên enthalpy chuẩn của phản ứng trên theo số liệu giá trị enthalpy tạo thành chuẩn của các hợp chất trong bảng sau đây. Cho biết phản ứng có thuận lợi về mặt năng lượng không.
|
Hợp chất |
CaSO3(s) |
CaCO3(s) |
SO2(g) |
CO2(g) |
|
ΔfHo298 |
- 1634,9 |
- 1207,6 |
- 296,8 |
- 393,5 |
c) Trong phản ứng trên, vì sao đá vôi phải được dùng ở dạng bột?
d) Calcium sulfite (CaSO3) thường được chuyển hoá thành thạch cao có công thức CaSO4.2H2O. Phản ứng hoá học chuyển CaSO3 thành CaSO4.2H2O có thuộc loại phản ứng oxi hoá – khử không?
Bài 21 :
: Một số quá trình tự nhiên và hoạt động của con người thải hydrogen sulfide vào không khí. Chất này có thể bị oxi hoá bởi oxygen có trong không khí theo hai phản ứng sau:
H2S(g) + \(\frac{3}{2}\)O2(g) → SO2(g) + H2O(g) (1)
H2S(g) +\(\frac{1}{2}\) O2(g) → S(s) + H2O(g) (2)
Cho biết giá trị enthalpy tạo thành chuẩn của H2S(g), SO2(g) và H2O(g) lần lượt là: –20,7 kJ mol−1; –296,8 kJ mol−1 và –241,8 kJ mol−1.
Bài 22 :
Cho giá trị enthalpy tạo thành chuẩn của khí SO2 và khí SO3 lần lượt là –296,8 kJ mol−1 và –395,7 kJ mol−1.
Tính giá trị biến thiên enthalpy chuẩn của phản ứng sau:
SO2(g) + \(\frac{1}{2}\)O2(g) → SO3(g)
Từ đó, hãy cho biết phản ứng trên có thuận lợi về mặt năng lượng không.
Bài 23 :
Trong phản ứng, SO2 có thể đóng vai trò là một oxide acid (acidic oxide). Hoàn thành các phương trình hoá học dưới đây để minh họa vai trò oxide acid của SO2.
a) Tan trong nước tạo thành acid yếu H2SO3.
b) Phản ứng với dung dịch base tạo muối và nước.
c) Phản ứng với oxide base (basic oxide) tạo muối.
Bài 24 :
Những ý kiến nào sau đây về sulfur dioxide (SO2) là đúng?
(a) Có độc tính đối với con người.
(b) Phản ứng được với đá vôi.
(c) Khí này được tạo thành từ hoạt động của núi lửa trong tự nhiên, từ quá trình đốt cháy nhiên liệu hóa thạch của con người,...
(d) Là oxide lưỡng tính.
Bài 25 :
Trái cây tươi cắt sẵn và đóng gói có thời hạn sử dụng ngắn. Sulfur dioxide thường được sử dụng để làm giảm sự thâm đen và sự phân huỷ, nhưng quá trình này gây nguy hiểm đến sức khoẻ của người tiêu dùng. Kĩ thuật đóng gói bổ sung khí (Modified Atmosphere Packaging – MAP) là một giải pháp an toàn thay thế. Hỗn hợp khí ở nhiệt độ thấp được sử dụng trong kĩ thuật MAP được trình bày như sau:
|
Sản phẩm |
%O2 (về thể tích) |
%CO2 (về thể tích) |
|
Táo |
4 |
2 |
|
Dâu tây |
2,5 |
16 |
|
Đậu Hà Lan |
9 |
7 |
|
Cần tây |
11 |
9 |
Bảng tổng hợp ở trên cho biết thành phần của hỗn hợp khí sử dụng đối với mỗi loại rau quả giúp chúng có thời hạn sử dụng lâu nhất. Khí còn lại là nitrogen.
a) Dựa vào bảng số liệu trên, hãy cho biết loại rau quả tươi nào ở trong bảng được đóng gói với hỗn hợp khí có thành phần N2 giống với không khí nhất?
A. Táo. B. Dâu tây. C. Đậu Hà Lan. D. Cần tây.
b) Thực tế, do lợi ích kinh tế trước mắt mà nhiều tổ chức, cá nhân đã sử dụng hoá chất độc hại để bảo quản trái cây. Việc dùng hoá chất làm cho trái cây giữ được rất lâu. Những giải pháp bảo quản trái cây nào được cho là an toàn và không an toàn với người dùng? Đánh dấu ✔ vào bảng sau ở ô thích hợp.
|
Giải pháp |
An toàn |
Không an toàn |
|
(1) Dùng hóa chất SO2 để bảo quản trái cây. |
|
|
|
(2) Bảo quản trái cây trong tủ lạnh. |
|
|
|
(3) Kĩ thuật đóng gói bổ sung khí MAP. |
|
|
Bài 26 :
Khí SO2 là một trong các chất chủ yếu gây ô nhiễm môi trường nhưng khi được sử dụng đúng mục đích sẽ có nhiều ứng dụng: dùng để sản xuất sulfuric acid, tẩy trắng giấy, bột giấy, chống nấm mốc cho lương thực, thực phẩm. Trong công nghiệp SO2 được sản xuất từ các nguyên liệu khác nhau như lưu huỳnh, đốt quặng pyrit sắt (FeS2). Hãy cho biết ưu và nhược điểm đối với môi trường khi điều chế SO2 từ 2 loại nguyên liệu trên?
Bài 27 :
Hãy cho biết người dân có thể đối mặt với những nguy cơ nào khi một nhà máy sản xuất lưu huỳnh bị cháy. Giải thích.
Bài 28 :
Khí thải của các nhà máy, xí nghiệp, ... có chứa nhiều SO2. Đây là một trong những nguyên nhân chủ yếu gây ra mưa acid, gây tổn hại cho nhiều công trình làm bằng sắt, đá. Hãy giải thích bằng các phương trình hoá học xảy ra (nếu có).
Bài 29 :
Cho các phương trình hoá học sau:
(1) SO2 + 2H2S → 3S + 2H2O
(2) SO2 + Br2+ 2H2O → 2HBr + H2SO4
Phát biểu nào sau đây đúng?
A. SO2 chỉ thể hiện tính oxi hoá.
B. SO2 chỉ thể hiện tính khử.
C. SO2 vừa thể hiện tính oxi hoá, vừa thể hiện tính khử.
D. SO2 không thể hiện tính khử và không thể hiện tính oxi hoá.
Bài 30 :
Chất khí (X) tan trong nước tạo ra dung dịch làm quỳ tím hóa đỏ và khí (X) có thể được dùng làm chất tẩy màu. Khí (X) là
A. NH3. B. CO2. C. SO2. D. O3.
Danh sách bình luận