Vận dụng kiến thức về cân bằng hoá học, tốc độ phản ứng, biến thiên enthalpy để giải thích các điều kiện của phản ứng sản xuất ammonia, cụ thể:
1. Nếu tăng hoặc giảm nhiệt độ sẽ ảnh hưởng đến sự chuyển dịch cân bằng và tốc độ phản ứng như thế nào?
2. Nếu giảm áp suất, cân bằng chuyển dịch theo chiều nào? Tại sao không thực hiện ở áp suất cao hơn?
3. Vai trò của chất xúc tác trong phản ứng là gì?
Trong công nghiệp, quá trình sản xuất ammonia thường được thực hiện ở nhiệt độ 400 °C – 450 °C, áp suất 150 – 200 bar, xúc tác Fe.
N2(g) + 3H2(g) ⇌ 2NH3(g) ΔrHo = -91,8 kJ
1. ΔrHo < 0 => phản ứng tỏa nhiệt => Tăng nhiệt độ thì cân bằng chuyển dịch theo chiều nghịch, giảm nhiệt độ thì cân bằng chuyển dịch theo chiều thuận. Tuy nhiên nếu ở nhiệt độ quá thấp thì tốc độ của phản ứng nhỏ, phản ứng diễn ra chậm nên thực tế, phản ứng xảy ra tốt nhất ở 400-450oC.
2. Số mol khí sau phản ứng nhỏ hơn số mol khí trước phản ứng nên giảm áp suất thì phản ứng chuyển dịch theo chiều nghịch.
Sản xuất ammonia ở áp suất 150 – 200 bar mà không thực hiện ở áp suất cao hơn.
Giải thích: khi tăng áp suất thì nồng độ NH3 tăng không nhiều, trong khi đó tiêu tốn năng lượng nhiều và yêu cầu thiết bị chịu được áp suất cao.
3. Việc sử dụng xúc tác bột sắt giúp phản ứng nhanh đạt trạng thái cân bằng.
Trong công nghiệp, quá trình sản xuất ammonia thường được thực hiện ở nhiệt độ 400 °C – 450 °C, áp suất 150 – 200 bar, xúc tác Fe.
N2(g) + 3H2(g) ⇌ 2NH3(g) ΔrHo = -91,8 kJ
1. Vì ΔrHo = -91,8 kJ < 0 nên phản ứng thuận toả nhiệt. Vậy:
+ Nếu tăng nhiệt độ, cân bằng chuyển dịch theo chiều nghịch (tức chiều phản ứng thu nhiệt) làm giảm hiệu suất phản ứng.
+ Nếu giảm nhiệt độ, cân bằng chuyển dịch theo chiều thuận (tức chiều phản ứng toả nhiệt) làm tăng hiệu suất phản ứng.
Tuy nhiên, khi thực hiện phản ứng ở nhiệt độ quá thấp thì tốc độ của phản ứng nhỏ, phản ứng diễn ra chậm. Thực tế, người ta đã chọn nhiệt độ phù hợp, khoảng 400 oC - 450 oC.
2. Khi giảm áp suất, cân bằng chuyển dịch theo chiều làm tăng áp suất của hệ - tức chiều làm tăng số mol khí, hay chiều nghịch.
Quá trình sản xuất NH3 được thực hiện ở áp suất 150 – 200 bar mà không thực hiện ở áp suất cao hơn. Điều này được giải thích như sau: Khi thực hiện ở áp suất cao sẽ thu được nồng độ NH3 tại thời điểm cân bằng lớn, tuy nhiên khi tăng áp suất thì sự tăng nồng độ NH3 không tăng nhanh chỉ tăng chậm. Ngoài ra, khi tăng áp suất thì tiêu tốn năng lượng và yêu cầu thiết bị phải chịu được áp suất cao, do đó phải tính toán chính xác khi tăng áp suất để mang lại hiệu quả kinh tế cao nhất. Thực tế chứng minh quá trình sản xuất NH3 được thực hiện ở áp suất 150 – 200 bar đem lại hiệu quả cao nhất.
3. Việc sử dụng chất xúc tác là bột sắt có tác dụng làm cho phản ứng nhanh đạt tới trạng thái cân bằng.














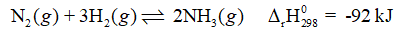 dịch theo chiều nào (có giải thích) khi:
dịch theo chiều nào (có giải thích) khi:




Danh sách bình luận