1. Sắp xếp các hợp chất sau vào vị trí tương ứng trong trục biểu diễn số oxi hóa của nitrogen: NO, N2O, NO2, NH3, HNO2, HNO3, NH4Cl, KNO2, NaNO3.
2. Dựa vào trục biểu diễn số oxi hóa của nitrogen để giải thích nitrogen có cả tính oxi hóa và tính khử. Viết một quá trình oxi hóa và một quá trình khử để mình họa.
1. \(\mathop {\rm{N}}\limits^{{\rm{ + 2}}} \mathop {\rm{O}}\limits^{{\rm{ - 2}}} {\rm{;}}{\mathop {{\rm{ N}}}\limits^{{\rm{ + 1}}} _{\rm{2}}}\mathop {\rm{O}}\limits^{{\rm{ - 2}}} {\rm{;}}\mathop {{\rm{ N}}}\limits^{{\rm{ + 4}}} {\mathop {\rm{O}}\limits^{{\rm{ - 2}}} _{\rm{2}}}{\rm{;}}\mathop {{\rm{ N}}}\limits^{{\rm{ - 3}}} {\mathop {\rm{H}}\limits^{{\rm{ + 1}}} _{\rm{3}}}{\rm{;}}\mathop {{\rm{ H}}}\limits^{{\rm{ + 1}}} \mathop {\rm{N}}\limits^{{\rm{ + 5}}} {\mathop {\rm{O}}\limits^{{\rm{ - 2}}} _{\rm{3}}};\mathop {\rm{N}}\limits^{{\rm{ - 3}}} \mathop {{{\rm{H}}_{\rm{4}}}}\limits^{{\rm{ + 1}}} \mathop {{\rm{Cl; }}}\limits^{{\rm{ - 1}}} \mathop {\rm{K}}\limits^{{\rm{ + 1}}} \mathop {\rm{N}}\limits^{{\rm{ + 3}}} \mathop {{{\rm{O}}_{\rm{2}}}}\limits^{{\rm{ - 2}}} {\rm{;}}\mathop {{\rm{Na}}}\limits^{{\rm{ + 1}}} \mathop {\rm{N}}\limits^{{\rm{ + 5}}} {\mathop {\rm{O}}\limits^{{\rm{ - 2}}} _{\rm{3}}}\)
2. Số oxi hóa của nitrogen có thể tăng, có thể giảm nên nitrogen có cả tính oxi hóa cả tính khử.
1.
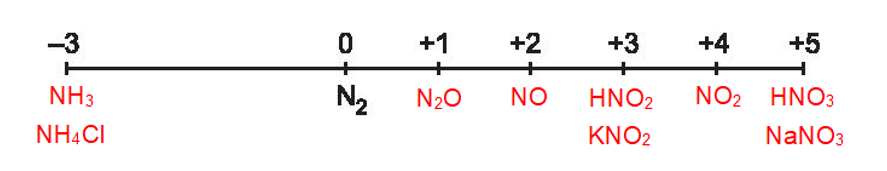
2. Khi tham gia phản ứng oxi hoá – khử, số oxi hoá của nitrogen có thể giảm hoặc tăng, do đó nitrogen thể hiện tính oxi hoá hoặc tính khử. Một số quá trình minh hoạ:
Quá trình oxi hoá: \(\mathop {{{\rm{N}}_{\rm{2}}}}\limits^{\rm{0}} \to {\rm{2}}\mathop {\rm{N}}\limits^{{\rm{ + 2}}} {\rm{ + 4e}}\)
Quá trình khử: \(\mathop {{{\rm{N}}_{\rm{2}}}}\limits^{\rm{0}} + {\rm{6e}} \to {\rm{2}}\mathop {\rm{N}}\limits^{ - 3} \)



















Danh sách bình luận