Cho cân bằng \(C{H_4}(g) + {H_2}O(g) \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over{\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} CO(g) + 3{H_2}(g)\). Khi giảm nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu đúng khi nói về cân bằng này là:
-
A.
Phản ứng thuận tỏa nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ
-
B.
Phản ứng nghịch tỏa nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ
-
C.
Phản ứng thuận thu nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ
-
D.
Phản ứng nghịch thu nhiệt, cân bằng dịch chuyển theo chiều thuận khi giảm nhiệt độ
Dựa vào kiến thức về nguyên lí chuyển dịch cân bằng Le Chatelier
Tỉ khối so với H2 giảm nên M trung bình giảm số mol tăng nên cân bằng chuyển dịch theo chiều thuận
Vậy khi giảm nhiệt độ thì cân bằng chuyển dịch theo chiều thuận (tỏa nhiệt)
Phản ứng thuận tỏa nhiệt; phản ứng nghịch thu nhiệt; cân bằng chuyển dịch theo chiều thuận khi giảm nhiệt độ
Đáp án D đúng
Đáp án : D
Ý nghĩa của hằng số cân bằng
KC càng lớn thì phản ứng thuận càng chiếm ưu thế hơn và ngược lại. KC càng nhỏ thì phản ứng nghịch càng chiếm ưu thế
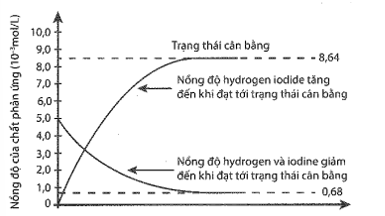
Tại thời điểm cân bằng hoá học thì:
- Phản ứng vẫn diễn ra với tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
- Nồng độ các chất không đổi, chứ không có bằng nhau.



















Danh sách bình luận