Để xác định nồng độ mol/l của dd K2Cr2O7 người ta làm như sau:
Lấy 10 ml dung dịch K2Cr2O7 cho tác dụng với lượng dư dung dịch KI trong môi trường axit sunfuric loãng dư. Lượng I2 thoát ra trong phản ứng được chuẩn độ bằng lượng vừa đủ là 18 ml dung dịch Na2S2O3 0,05M.
Biết các phản ứng hóa học xảy ra:
(1) 6KI + K2Cr2O7 + 7H2SO4 → 4K2SO4 + Cr2(SO4)3 + 3I2 + 7H2O;
(2) I2 + 2Na2S2O3 → 2NaI + Na2S4O6.
Nồng độ mol/l của K2Cr2O7 là
-
A.
0,02M.
-
B.
0,03M.
-
C.
0,015M.
-
D.
0,01M.
Bước 1: Tính số mol của Na2S2O3
Bước 2: Viết phương trình phản ứng
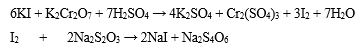
Bước 3: Tính CM của K2Cr2O7
- Theo PTHH, từ số mol của Na2S2O3
→ Số mol I2 → Số mol K2Cr2O7
→ CM của K2Cr2O7
Bước 1: Tính số mol của Na2S2O3
nNa2S2O3 = 0,018.0,05 = 9.10-4 mol
Bước 2: Viết phương trình phản ứng, tính số mol các chất theo PTHH
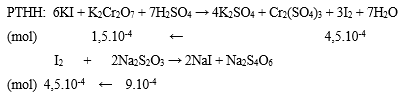
Bước 3: Tính CM của K2Cr2O7
⟹ CM K2Cr2O7 = 1,5.10-4/0,01 = 0,0015M.
Đáp án : C



















Danh sách bình luận