Để xác định nồng độ dung dịch NaOH người ta tiến hành như sau: Cân 1,26 gam axit oxalic ngậm nước (H2C2O4.2H2O) hòa tan hoàn toàn vào nước, định mức thành 100 ml. Lấy 10 ml dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH = 9) thì hết 17,5 ml dung dịch NaOH. Tính nồng độ dung dịch NaOH đã dùng.
-
A.
0,1143M.
-
B.
0,2600M.
-
C.
0,1240M.
-
D.
0,1600M.
Bước 1: Tính n(COOH)2 trong 10 ml dung dịch axit oxalic
- Tính nH2C2O4.2H2O
- 100 ml dd axit oxalic chứa 0,01 mol (COOH)2
10 ml ⟶ x mol (COOH)2
Bước 2: Tính nNaOH
- pH > 7 ⟹ NaOH dư, (COOH)2 hết
- Đặt nNaOH = x mol.
- PTHH: (COOH)2 + 2NaOH ⟶ (COONa)2 + 2H2O
Sau phản ứng xác định số mol NaOH dư.
- pH = 9 ⟹ [OH-]sau pư ⟹ x
Bước 3: Tính CM NaOH
Bước 1: Tính n(COOH)2 trong 10 ml dung dịch axit oxalic
- \({n_{{H_2}{C_2}{O_4}.2{H_2}O}} = \dfrac{{1,26}}{{90 + 18.2}} = 0,01\left( {mol} \right)\)
- 100 ml dung dịch axit oxalic chứa 0,01 mol (COOH)2
10 ml ⟶ 0,001 mol
Bước 2: Tính nNaOH
- Phenolphtalein xuất hiện màu hồng ở pH = 9 > 7 ⟹ NaOH dư, (COOH)2 hết
- Đặt nNaOH = x mol.
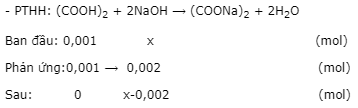
pH = 9 ⟹ pOH = 14 - 9 = 5 ⟹ [OH-]sau pư = 10-5
Bước 3: Tính CM NaOH
- Ta có: \({\left[ {O{H^ - }} \right]_{sau\,pu}} = \dfrac{{x - 0,002}}{{(10 + 17,5){{.10}^{ - 3}}}} = {10^{ - 5}}\) ⟹ x = 2,000275.10-3.
⟹ CM NaOH = \(\dfrac{{{n_{NaOH}}}}{{{V_{dd\,NaOH}}}}\) = \(\dfrac{{2,{{000275.10}^{ - 3}}}}{{17,{{5.10}^{ - 3}}}}\) = 0,1143 M.
Đáp án : A



















Danh sách bình luận