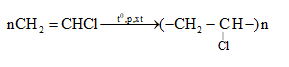Đề thi thử THPT QG môn Hóa trường THPT chuyên Vĩnh PhúcĐề bài
Câu 1 :
Kim loại nào sau đây được điều chế bằng phản ứng nhiệt luyện?
Câu 2 :
Kim loại nào sau đây thuộc nhóm IIA?
Câu 3 :
Cho 0,9 gam glucozo (C6H12O6) tác dụng hết với lượng dư dung dịch AgNO3 trong NH3, thu được m gam Ag. Giá trị của m là
Câu 4 :
Cho dung dịch KOH vào dung dịch chất X, thu được kết tủa màu xanh lam. Chất X là
Câu 5 :
Isoamylaxetat là este có mùi chuối chín. Công thức của isoamylaxetat là
Câu 6 :
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hợp khí X. Cho toàn bộ X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Câu 7 :
Chất nào sau đây thuộc loại đisaccarit?
Câu 8 :
Thủy phân hoàn toàn 1 mol peptit mạch hở X, thu được 2 mol Gly, 2 mol Ala và 1 mol Val. Mặt khác, thủy phân hoàn toàn X, thu được hỗn hợp các amino axit và các peptit (trong đó có Gly-Ala-Val). Số công thức cấu tạo phù hợp với tính chất của X là
Câu 9 :
Kim loại Cu tan được trong dung dịch nào sau đây?
Câu 10 :
Tiến hành các thí nghiệm sau: (a) Nhúng thanh đồng nguyên chất vào dung dịch FeCl3. (b) Cắt miếng sắt tây (sắt tráng thiếc), để trong không khí ẩm. (c) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịch CuSO4. (d) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc đựng dung dịch NaCl. Trong các thí nghiệm trên, số thí nghiệm chỉ xảy ra ăn mòn điện hóa học là
Câu 11 :
Polivinylclorua (PVC) được điều chế từ phản ứng trùng hợp chất nào sau đây?
Câu 12 :
Thực hiện các thí nghiệm sau: (a) Cho dung dịch HCl vào dung dịch NaAlO2 dư. (b) Cho Al2S3 vào dung dịch HCl dư. (c) Cho Al vào dung dịch NaOH. (d) Cho dung dịch NH3 vào dung dịch AlCl3. (e) Cho khí CO2 vào dung dịch NaAlO2. (g) Cho kim loại Al vào dung dịch FeCl3 dư. Sau khi kết thúc các phản ứng, số thí nghiệm thu được kết tủa là
Câu 13 :
Công thức hóa học của polietilen (PE) là
Câu 14 :
Oxit nào sau đây được dùng để luyện gang thép?
Câu 15 :
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất
Câu 16 :
Cho 15 gam hỗn hợp gồm hai amin đơn chức tác dụng vừa đủ với V ml dung dịch HCl 0,75M, thu được dung dịch chứa 23,76 gam hỗn hợp muối. Giá trị của V là
Câu 17 :
Khi cho Fe vào dung dịch hỗn hợp các muối AgNO3, Cu(NO3)2, Pb(NO3)2 thì Fe sẽ khử ion kim loại theo thứ tự sau (ion đặt trước sẽ bị khử trước):
Câu 18 :
Đốt cháy hoàn toàn a gam hỗn hợp các este no, đơn chức, mạch hở. Sản phẩm cháy được dẫn vào bình đựng nước vôi trong, thấy khối lượng bình tăng 6,2 gam. Số mol CO2 và H2O sinh ra lần lượt là
Câu 19 :
Dung dịch Ala-Val phản ứng được với dung dịch nào sau đây?
Câu 20 :
Thủy phân hoàn toàn tinh bột thu được monosaccarit X. Hidro hóa X thu được chất hữu cơ Y. Hai chất X,Y lần lượt là
Câu 21 :
Đun hợp chất hữu cơ X (C5H11O2N) với dung dịch NaOH, thu được C2H4O2NNa và chất hữu cơ Y. Cho hơi Y qua CuO/to, thu được chất hữu cơ Z có khả năng cho phản ứng tráng gương. Công thức cấu tạo của X là
Câu 22 :
Hỗn hợp X gồm axit pamitic, axit stearic và triglixerit Y. Đốt cháy hoàn toàn m gam X, thu được 1,56 mol CO2 và 1,52 mol H2O. Mặt khác, m gam X tác dụng vừa đủ với 0,09 mol NaOH trong dung dịch, thu được glixerol và dung dịch chỉ chứa a gam hỗn hợp muối natri panmitat, natri stearat. Giá trị của a là
Câu 23 :
Các sơ đồ phản ứng theo đúng tỉ lệ mol: (a) X + 2NaOH \(\xrightarrow{{{t^o}}}\)X1 + 2X2 (b) X1 + H2SO4 → X3 + Na2SO4 (c) nX3 + nX4 \(\xrightarrow{{{t^o},xt}}\)poli(etylenterephtalat) + 2nH2O (d) X2 + CO \(\xrightarrow{{{t^o},xt}}\)X5 (e) X4 + 2X5 \(\overset {{H_2}S{O_4}\,dac,{t^o}} \leftrightarrows \)X6 + 2H2O Cho biết X là este có công thức phân tửu C10H10O4; X1, X2, X3, X4, X5, X6 là các hợp chất hữu cơ khác nhau. Phân tử khối của X6 là
Câu 24 :
Hỗn hợp E gồm chất X (CmH2m+4O4N2, là muối của axit cacboxylic hai chức) và chất Y (CnH2n+3O2N, là muối của axit cacboxylic đơn chức). Đốt cháy hoàn toàn 0,1 mol E cần vừa đủ 0,26 mol O2, thu được N2,CO2 và 0,4 mol H2O. Mặt khác, cho 0,1 mol E tác dụng hết với dung dịch NaOH, cô cạn dung dịch sau phản ứng, thu được hỗn hợp hai chất khí đều làm xanh qùy tím ẩm và a gam hỗn hợp hai muối khan. Giá trị của của a là
Câu 25 :
Cho dung dịch metyl amin dư lần lượt vào các dung dịch riêng biệt sau: AlCl3, FeCl3, Zn(NO3)2, Cu(NO3)2, HCl, Na2SO4. Sau khi các phản ứng kết thúc, số kết tủa thu được là
Câu 26 :
Cho X, Y là hai axit cacboxylic đơn chức (MX < MY); T là este ba chức, mạch hở được tạo bởi X, Y với glixerol. Cho 23,06 gam hỗn hợp E gồm X, Y, T và glixerol (với số mol của X bằng 8 lần số mol của T) tác dụng vừa đủ với 200 ml dung dịch NaOH 2M, thu được hỗn hợp F gồm hai muối có tỉ lệ mol 1 : 3 và 3,68 gam glixerol. Đốt cháy hoàn toàn F cần vừa đủ 0,45 mol O2, thu được Na2CO3, H2O và 0,4 mol CO2. Phần trăm khối lượng của T trong E có giá trị gần nhất với giá trị nào sau đây?
Câu 27 :
Hỗn hợp E gồm bốn este đều có công thức C8H8O2 và có vòng benzen. Cho 16,32 gam E tác dụng tối đa với V ml dung dịch NaOH 1M (đun nóng), thu được hỗn hợp X gồm các ancol và 18,78 gam hỗn hợp muối. Cho toàn bộ X vào bình đựng kim loại Na dư, sau khi phản ứng kết thúc khối lượng chất rắn trong bình tăng 3,83 gam so với ban đầu. Giá trị của V là
Câu 28 :
Cho X, Y, Z là 3 peptit mạch hở (phân tử có số nguyên tử cacbon tương ứng 8, 9, 11; Z có nhiều hơn Y một liên kết peptit); T là este no, đơn chức, mạch hở. Chia 249,56 gam hỗn hợp E gồm X, Y, Z, T thành hai phần bằng nhau. Đốt cháy hoàn toàn phần một, thu dược a mol CO2 và (a-0,11) mol H2O. Thủy phân hoàn toàn phần hai bằng dung dịch NaOH vừa đủ, thu được ancol etylic và 133,18 gam hỗn hợp G (gồm 4 muối của Gly, Ala, Val và axit cacboxylic). Đốt cháy hoàn toàn G, cần vừa đủ 3,385 mol O2. Phần trăm khối lượng của Y trong E là
Câu 29 :
Poli(metyl metacrylat) và nilon-6 được tạo thành từ các monome tương ứng là
Câu 30 :
Este X có công thức phân tử C6H10O4. Xà phòng hóa hoàn toàn X bằng dung dịch NaOH, thu được ba chất hữu cơ Y, Z, T. Biết Y tác dụng với Cu(OH)2 tạo dung dịch màu xanh lam. Nung nóng Z với hỗn hợp rắn gồm NaOH và CaO, thu được CH4. Phát biều nào sau đây sai?
Câu 31 :
Khi nghiên cứu cacbohidrat X ta nhận thấy: - X không tráng gương, có một đồng phân - X thủy phân trong nước được hai sản phẩm. Vậy X là
Câu 32 :
Cho các phát biểu sau: (a) Sau khi mổ cá, có thể dùng chanh để giảm mùi tanh. (b) Dầu thực vật và dầu nhớt bôi trơn máy đều có thành phần chính là chất béo. (c) Cao su thiên nhiên là polime của isopren. (d) Khi làm trứng muối (ngâm trứng trong dung dịch NaCl bão hòa) xảy ra hiện tượng đông tụ protein. (e) Thành phần chính của tóc là protein. (g) Để giảm đau nhức khi bị kiến đốt, có thể bôi giấm vào vết đốt. Số phát biểu đúng là
Câu 33 :
Cho 0,1 mol chất X có công thức là C2H12O4N2S tác dụng với dung dịch chứa 0,35 mol NaOH đun nóng thu được chất khí làm xanh giấy quỳ ẩm và dung dịch Y. Cô cạn dung dịch Y, thu được m gam chất rắn khan. Giá trị của m là
Câu 34 :
Cho hỗn hợp E gồm 0,1 mol X (C5H11O4N) và 0,15 mol Y (C5H14O4N2, là muối của axit cacboxylic hai chức) tác dụng hoàn toàn với dung dịch KOH, thu được một ancol đơn chức, hai amin no (kế tiếp trong dãy đồng đẳng) và dung dịch T. Cô cạn T, thu được hỗn hợp G gồm ba muối khan có cùng số nguyên tử cacbon trong phân tử (trong đó có hai muối của hai axit cacboxylic và muối của một α-amino axit). Phần trăm khối lượng của muối có phân tử khối lớn nhất trong G là
Câu 35 :
Thủy phân hoàn toàn a gam triglixerit X trong dung dịch NaOH, thu được glixerol và dung dịch chứa m gam hỗn hợp muối (gồm natri stearat; natri panmitat và C17HyCOONa). Đốt cháy hoàn toàn a gam X cần 1,55 mol O2, thu được H2O và 1,1 mol CO2. Giá trị của m là
Câu 36 :
Cho sơ đồ chuyển hóa sau: (1) n-pentan \(\xrightarrow{{{t^o}}}\) A + B và D + E (2) A + Cl2 \(\xrightarrow{{a/s}}\) CH3-CHCl-CH3 + F (3) CH3COONa + NaOH → D + G (4) D + Cl2 \(\xrightarrow{{a/s}}\) L + F (5) CH3-CHCl-CH3 + L + Na → M + NaCl Các chất A, B, D, E và M lần lượt có cấu tạo là
Câu 37 :
Hỗn hợp E gồm ba este mạch hở, đều có bốn liên kết π trong phân tử, trong đó có một este đơn chức là este của axit metacrylic và hai este hai chức là đồng phân của nhau. Đốt cháy hoàn toàn 12,22 gam E bằng O2, thu được 0,37 mol H2O. Mặt khác, cho 0,36 mol E phản ứng vừa đủ với 234 ml dung dịch NaOH 2,5M, thu được hỗn hợp X gồm các muối của các axit cacboxylic không no, có cùng số nguyên tử cacbon trong phân tử; hai ancol không no, đơn chức có khối lượng m1 gam và một ancol no, đơn chức có khối lượng m2 gam. Tỉ lệ m1 : m2 có giá trị gần nhất với giá trị nào sau đây?
Câu 38 :
Hỗn hợp X gồm alanin, axit glutamic và axit acrylic. Hỗn hợp Y gồm propen và trimetylamin. Đốt cháy hoàn toàn a mol X và b mol Y thì tổng số mol oxi cần dùng vừa đủ là 1,14 mol, thu được H2O, 0,1 mol N2 và 0,91 mol CO2. Mặt khác, khi cho a mol X tác dụng với dung dịch KOH dư thì lượng KOH phản ứng là m gam. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Câu 39 :
Cho các phát biểu sau: (a) Đipeptit Val-Lys có phản ứng màu biure. (b) Dung dịch axit glutamic đổi màu quỳ tím thành xanh. (c) Etyl fomat và glucozo có cùng công thức đơn giản nhất. (d) Phenylamin có lực bazo mạnh hơn amoniac. (e) Saccarozo có phản ứng thủy phân trong môi trường axit. (g) Vinyl axetat làm mất màu dung dịch brom. Số phát biểu đúng là
Câu 40 :
Cho các phát biểu sau: (a) Thủy phân triolein, thu được etylen glicol. (b) Tinh bột bị thủy phân khi có xúc tác axit hoặc enzim. (c) Thủy phân vinyl fomat, thu được hai sản phẩm đều có phản ứng tráng bạc. (d) Trùng ngưng ε-aminocaproic, thu được policaproamit. (e) Chỉ dùng quỳ tím có thể phân biệt ba dung dịch: alanin, lysin, axit glutamic. (f) Phenylamin tan ít trong nước nhưng tan tốt trong dung dịch HCl. Số phát biểu đúng là
Lời giải và đáp án
Câu 1 :
Kim loại nào sau đây được điều chế bằng phản ứng nhiệt luyện?
Đáp án : B Phương pháp giải :
Phương pháp nhiệt luyện:dùng các chất khử như C, H2, CO, Al để khử các oxi kim loại có tính khử trung bình để điều chế kim loại. (Các kim loại đứng sau Al) Lời giải chi tiết :
Fe có thể được điều chế bằng phương pháp nhiệt luyện VD: H2 + FeO \(\xrightarrow{{{t^o}}}\) Fe + H2O
Câu 2 :
Kim loại nào sau đây thuộc nhóm IIA?
Đáp án : D Lời giải chi tiết :
Na là kim loại thuộc nhóm IA Al là kim loại thuộc nhóm IIIA Fe là kim loại thuộc nhóm VIIIB Ca là kim loại thuộc nhóm IIA
Câu 3 :
Cho 0,9 gam glucozo (C6H12O6) tác dụng hết với lượng dư dung dịch AgNO3 trong NH3, thu được m gam Ag. Giá trị của m là
Đáp án : D Phương pháp giải :
1 mol glucozo tráng bạc cho 2 mol Ag C6H12O6 → 2Ag Lời giải chi tiết :
nC6H12O6 = 0,9:180 = 0,005 (mol) C6H12O6 → 2Ag 0,005 → 0,01 (mol) => mAg = 0,01.108 = 1,08 (g)
Câu 4 :
Cho dung dịch KOH vào dung dịch chất X, thu được kết tủa màu xanh lam. Chất X là
Đáp án : A Phương pháp giải :
Dựa vào màu sắc kết tủa của các hiđroxit Lời giải chi tiết :
2KOH + CuCl2 → KCl + Cu(OH)2↓xanh lam 2KOH + FeCl2 → KCl + Fe(OH)2↓ trắng xanh 2KOH + MgCl2 → KCl + Mg(OH)2↓trắng 3KOH + FeCl3 → KCl + Fe(OH)3↓ nâu đỏ
Câu 5 :
Isoamylaxetat là este có mùi chuối chín. Công thức của isoamylaxetat là
Đáp án : A Phương pháp giải :
Từ tên gọi của este dịch ra CTCT của este tên este RCOOR' = tên gốc R' + tên gốc RCOO + at Lời giải chi tiết :
Công thức của isoamylaxetat là CH3COOCH2CH2CH(CH3)2.
Câu 6 :
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hợp khí X. Cho toàn bộ X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Đáp án : A Phương pháp giải :
BTNT C: nCaCO3 = nCO2 = nO(trong CuO) Lời giải chi tiết :
nCuO = 8 : 80 = 0,1 (mol) CO + CuO \(\xrightarrow{{{t^0}}}\) Cu + CO2 0,1 → 0,1 (mol) Hỗn hợp khí X có CO2 và CO dư, khi cho qua dung dịch nước vôi trong dư chỉ có CO2 tham gia phản ứng CO2 + Ca(OH)2 → CaCO3↓ + H2O 0,1 → 0,1 (mol) => mkết tủa = mCaCO3 = 0,1.100 = 10 (g)
Câu 7 :
Chất nào sau đây thuộc loại đisaccarit?
Đáp án : C Phương pháp giải :
Thuộc phân loại cacbohiđrat: mono saccarit, đisaccarit, polisaccarit.
Lời giải chi tiết :
Xenlulozo, Tinh bột thuộc polisaccarit Glucozơ thuộc monosaccarit Saccarozơ thuộc đisaccarit
Câu 8 :
Thủy phân hoàn toàn 1 mol peptit mạch hở X, thu được 2 mol Gly, 2 mol Ala và 1 mol Val. Mặt khác, thủy phân hoàn toàn X, thu được hỗn hợp các amino axit và các peptit (trong đó có Gly-Ala-Val). Số công thức cấu tạo phù hợp với tính chất của X là
Đáp án : B Phương pháp giải :
X là pentapeptit. Vì thủy phân không hoàn toàn thu được peptit: Gly- Ala - Val => giữ nguyên mạch tripeptit này, thêm Gly và Ala vào các vị trí sao cho tạo thành các pentapetit khác nhau. Lời giải chi tiết :
Các CTCT phù hợp là: Gly - Gly- Ala - Val- Ala Ala - Gly- Ala - Val- Gly Gly- Ala - Val- Gly - Ala Gly- Ala - Val- Ala - Gly Ala - Gly-Gly- Ala - Val Gly - Ala - Gly- Ala - Val => Có 6 CTCT thỏa mãn
Câu 9 :
Kim loại Cu tan được trong dung dịch nào sau đây?
Đáp án : C Phương pháp giải :
Dựa vào tính chất hóa học của Cu trong sgk hóa 12 Lời giải chi tiết :
Cu tan được trong dd HNO3 VD: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Câu 10 :
Tiến hành các thí nghiệm sau: (a) Nhúng thanh đồng nguyên chất vào dung dịch FeCl3. (b) Cắt miếng sắt tây (sắt tráng thiếc), để trong không khí ẩm. (c) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịch CuSO4. (d) Quấn sợi dây đồng vào đinh sắt rồi nhúng vào cốc đựng dung dịch NaCl. Trong các thí nghiệm trên, số thí nghiệm chỉ xảy ra ăn mòn điện hóa học là
Đáp án : B Phương pháp giải :
ăn mòn hóa học: là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường. ăn mòn điện hóa học: là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương Điều kiện xảy ra ăn mòn điện hóa học là: + Xuất hiện ít nhất 2 cặp điện cực khác nhau về bản chất như: KL-KL ; KL- PK; KL- HC + Các chất phải tiếp xúc trực tiếp hoặc gián tiếp với nhau thông qua dây dẫn + Cùng nhúng trong 1 dung dịch chất điện li Lời giải chi tiết :
(a) chỉ xảy ra ăn mòn hóa học (b) xảy ra cả ăn mòn hóa học và ăn mòn điện hóa học (c) xảy ra ăn mòn hóa học và điện hóa học (d) Chỉ xảy ra ăn mòn điện hóa học Vậy chỉ có 1 thí nghiệm (d) xảy ra ăn mòn điện hóa học
Câu 11 :
Polivinylclorua (PVC) được điều chế từ phản ứng trùng hợp chất nào sau đây?
Đáp án : B Lời giải chi tiết :
PVC được điều chế từ CH2=CHCl
Câu 12 :
Thực hiện các thí nghiệm sau: (a) Cho dung dịch HCl vào dung dịch NaAlO2 dư. (b) Cho Al2S3 vào dung dịch HCl dư. (c) Cho Al vào dung dịch NaOH. (d) Cho dung dịch NH3 vào dung dịch AlCl3. (e) Cho khí CO2 vào dung dịch NaAlO2. (g) Cho kim loại Al vào dung dịch FeCl3 dư. Sau khi kết thúc các phản ứng, số thí nghiệm thu được kết tủa là
Đáp án : C Phương pháp giải :
Viết các phản ứng hóa học xảy ra, chọn các thí nghiệm có xuất hiện kết tủa Chý ý đến các chất tham gia phản ứng, chất cho hết dư Lời giải chi tiết :
(a) 6HCl dư+ 3NaAlO2 → 3NaCl + AlCl3 + 3H2O (b) Al2S3 + 6HCl dư → 2AlCl3 + 3H2S↑ (c) Al + NaOH + H2O → NaAlO2 + 3/2H2 (d) 3NH3 + 3H2O + AlCl3 → Al(OH)3↓ + 3NH4Cl (e) CO2 + H2O + NaAlO2 → Al(OH)3↓ + NaHCO3 (g) Al + 3FeCl3 dư → AlCl3 + 3FeCl2 => có 2 thí nghiệm (d) và (g) thu được kết tủa
Câu 13 :
Công thức hóa học của polietilen (PE) là
Đáp án : B Lời giải chi tiết :
Công thức hóa học của polietilen (PE) là [-CH2-CH2-]n
Câu 14 :
Oxit nào sau đây được dùng để luyện gang thép?
Đáp án : B Phương pháp giải :
Gang, thép là hợp kim của sắt và cacbon Lời giải chi tiết :
Fe2O3 là oxit dùng để luyện gang , thép
Câu 15 :
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất
Đáp án : D Phương pháp giải :
Dựa vào kiến thức được học về đại cương kim loại trong sgk hóa 12 Lời giải chi tiết :
Hg là kim loại có nhiệt độ nóng chảy thấp nhất
Câu 16 :
Cho 15 gam hỗn hợp gồm hai amin đơn chức tác dụng vừa đủ với V ml dung dịch HCl 0,75M, thu được dung dịch chứa 23,76 gam hỗn hợp muối. Giá trị của V là
Đáp án : D Phương pháp giải :
Bảo toàn khối lượng ta có: mHCl = mmuối - mRNH2 = ? Từ đó tính được nHCl và VHCl Lời giải chi tiết :
Đặt công thức của 2 amin đơn chức là RNH2 RNH2 + HCl → RNH3Cl Bảo toàn khối lượng ta có: mHCl = mmuối - mRNH2 = 23,76 - 15 = 8,76 (g) => nHCl = 8,76:36,5 = 0,24 (mol) => VHCl = n : CM = 0,24 : 0,75 = 0,32 (lít) = 320 (ml)
Câu 17 :
Khi cho Fe vào dung dịch hỗn hợp các muối AgNO3, Cu(NO3)2, Pb(NO3)2 thì Fe sẽ khử ion kim loại theo thứ tự sau (ion đặt trước sẽ bị khử trước):
Đáp án : A Phương pháp giải :
Ghi nhớ dãy điện hóa học của kim loại Fe sẽ khử cation kim loại mà kim loại của nó có tính khử yếu trước
Lời giải chi tiết :
Thứ tự khử: Fe khử Ag+, Cu2+ rồi đến Pb2+
Câu 18 :
Đốt cháy hoàn toàn a gam hỗn hợp các este no, đơn chức, mạch hở. Sản phẩm cháy được dẫn vào bình đựng nước vôi trong, thấy khối lượng bình tăng 6,2 gam. Số mol CO2 và H2O sinh ra lần lượt là
Đáp án : A Phương pháp giải :
- Đốt cháy este no, đơn chức: \({n_{C{O_2}}} = {\text{ }}{n_{{H_2}O}}\) \({m_ \uparrow } = {m_{C{O_2}}} + {m_{{H_2}O}}\)
Lời giải chi tiết :
- Đốt cháy este no đơn chức:\({n_{C{O_2}}} = {\text{ }}{n_{{H_2}O}} = a\,mol\) \( {\text{ }}{m_ \uparrow } = {\text{ }}{m_{C{O_2}}} + {\text{ }}{m_{{H_2}O\;}}\) \(< = > 6,2{\text{ }} = 44.a + 18.a{\text{ }}\) \( = > a = 0,1\,mol\)
Câu 19 :
Dung dịch Ala-Val phản ứng được với dung dịch nào sau đây?
Đáp án : D Lời giải chi tiết :
dd Ala - Val phản ứng được với dd H2SO4
Câu 20 :
Thủy phân hoàn toàn tinh bột thu được monosaccarit X. Hidro hóa X thu được chất hữu cơ Y. Hai chất X,Y lần lượt là
Đáp án : A Lời giải chi tiết :
Ta có (C6H10O5)n + nH2O → nC6H12O6 ( glucozo – X ) C6H12O6 + H2 → C6H14O6 ( sorbitol – Y )
Câu 21 :
Đun hợp chất hữu cơ X (C5H11O2N) với dung dịch NaOH, thu được C2H4O2NNa và chất hữu cơ Y. Cho hơi Y qua CuO/to, thu được chất hữu cơ Z có khả năng cho phản ứng tráng gương. Công thức cấu tạo của X là
Đáp án : C Phương pháp giải :
X (C5H11O2N) có dạng CnH2n+1O2N có phản ứng với NaOH => X có thể là + amino axit + este của axit cacboxylic với amin + este của aminoaxit với ancol Lời giải chi tiết :
Y là ancol bậc 1, Z là anđehit X (C5H11O2N) + NaOH → C2H4O2NNa + Y (ancol bậc 1) => X là este của aminoaxit với ancol => CTCT của X là: NH2CH2COOCH2-CH2-CH3 NH2CH2COOCH2-CH2-CH3 + NaOH → NH2CH2COONa + CH3CH2CH2OH(Y) CH3CH2CH2OH + 2CuO CH3CH2CH=O(Z) + Cu2O + H2O CH3CH2CH=O + 2AgNO3 + 3NH3 + H2O CH3CH2COONH4 + 2Ag↓ + 2NH4NO3
Câu 22 :
Hỗn hợp X gồm axit pamitic, axit stearic và triglixerit Y. Đốt cháy hoàn toàn m gam X, thu được 1,56 mol CO2 và 1,52 mol H2O. Mặt khác, m gam X tác dụng vừa đủ với 0,09 mol NaOH trong dung dịch, thu được glixerol và dung dịch chỉ chứa a gam hỗn hợp muối natri panmitat, natri stearat. Giá trị của a là
Đáp án : C Phương pháp giải :
nY = (nCO2 - nH2O)/2 = ? ∑ nCOO = nNaOH = 0,09 (mol) Bảo toàn khối lượng ta có: mX = mC + mH + mO = ? (g) Khi phản ứng với NaOH số mol H2O sinh ra = nCOOH(trong axit) = ? (mol) BTKL ta có: mX + mNaOH = mhh muối + mglixerol + mH2O => mmuối = ? Lời giải chi tiết :
Vì X + NaOH thu được glixerol và hỗn hợp muối natri panmitat, natri stearat => triglixerit Y là este no, ba chức, mạch hở Đốt cháy axit panmitic và axit stearic đều thu được nH2O = nCO2 => Sự chênh lệch mol H2O và CO2 là do đốt cháy Y Y có độ bất bão hòa k = 3 \({n_Y} = \frac{{{n_{C{O_2}}} - {n_{{H_2}O}}}}{{k - 1}} = \frac{{1,56 - 1,52}}{{3 - 1}} = 0,02\,\,(mol)\) Ta có: ∑ nCOO = nNaOH = 0,09 (mol) => nO (trong X) = 2nCOO = 0,18 (mol) => nCOOH- (trong axit) = ∑ nCOO - nCOO(trongY) = 0,09 - 0,02.3 = 0,03 (mol) Bảo toàn khối lượng ta có: mX = mC + mH + mO = 1,56.12 + 1,52.2 + 0,18.16 = 24,64 (g) Đặt công thức chung của Y là: (RCOO)3C3H5: 0,02 (mol) => nC3H5(OH)3= nY = 0,02 (mol) Khi phản ứng với NaOH số mol H2O sinh ra = nCOOH(trong axit) = 0,03 (mol) BTKL ta có: mX + mNaOH = mhh muối + mglixerol + mH2O => 24,64 + 0,09.40 = a + 0,02.92 + 0,03.18 => a = 25,86 (g)
Câu 23 :
Các sơ đồ phản ứng theo đúng tỉ lệ mol: (a) X + 2NaOH \(\xrightarrow{{{t^o}}}\)X1 + 2X2 (b) X1 + H2SO4 → X3 + Na2SO4 (c) nX3 + nX4 \(\xrightarrow{{{t^o},xt}}\)poli(etylenterephtalat) + 2nH2O (d) X2 + CO \(\xrightarrow{{{t^o},xt}}\)X5 (e) X4 + 2X5 \(\overset {{H_2}S{O_4}\,dac,{t^o}} \leftrightarrows \)X6 + 2H2O Cho biết X là este có công thức phân tửu C10H10O4; X1, X2, X3, X4, X5, X6 là các hợp chất hữu cơ khác nhau. Phân tử khối của X6 là
Đáp án : A Phương pháp giải :
Từ (b) suy ra X3 là axit Từ (c) suy ra X3 là axit terephtalat; X4 là etylenglicol) từ đó suy ra các chất còn lại Lời giải chi tiết :
Từ (b) suy ra X3 là axit Từ (c) suy ra X3 là axit terephtalat; X4 là etylenglicol) X3: HOOC-C6H4-COOH ; X4: HOCH2-CH2OH Từ (b) suy ra X1 là: NaOOC- C6H4-COONa X: C10H10O4 có k = (10.2+ 2-10)/2 = 6 Từ (a) suy ra X là este 2 chức => CTCT X: CH3OOC- C6H4-COOCH3 (a) CH3OOC- C6H4-COOCH3 (X) + 2NaOH \(\xrightarrow{{{t^o}}}\) NaOOC- C6H4-COONa (X1) + 2CH3OH (X2) (b) NaOOC- C6H4-COONa (X1) + H2SO4 → HOOC- C6H4-COOH (X3) + Na2SO4 (c) n HOOC- C6H4-COOH (X3) + nHOCH2-CH2OH (X4) \(\xrightarrow{{{t^o},xt}}\) poli(etylenterephtalat) + 2nH2O (d) CH3OH (X2)+ CO \(\xrightarrow{{{t^o},xt}}\) CH3COOH (X5) (e) HOCH2-CH2OH (X4) + 2CH3COOH (X5) \(\overset {{H_2}S{O_4}\,dac,{t^o}} \leftrightarrows \) CH3COO-CH2-CH2-OOCCH3 (X6) + 2H2O Vậy phân tử khối của X6 là 146
Câu 24 :
Hỗn hợp E gồm chất X (CmH2m+4O4N2, là muối của axit cacboxylic hai chức) và chất Y (CnH2n+3O2N, là muối của axit cacboxylic đơn chức). Đốt cháy hoàn toàn 0,1 mol E cần vừa đủ 0,26 mol O2, thu được N2,CO2 và 0,4 mol H2O. Mặt khác, cho 0,1 mol E tác dụng hết với dung dịch NaOH, cô cạn dung dịch sau phản ứng, thu được hỗn hợp hai chất khí đều làm xanh qùy tím ẩm và a gam hỗn hợp hai muối khan. Giá trị của của a là
Đáp án : D Phương pháp giải :
Viết phương trình đốt cháy CmH2m+4O4N2 + (1,5m-1)O2 → mCO2 + (m+2)H2O + N2 a → (1,5m-1)a → (m+2)a mol CnH2n+3O2N + (1,5n-0,25)O2 → nCO2 + (n+1,5)H2O + N2 b → (1,5n-0,25)b → (n+1,5)b mol Ta có hệ 3 phương trình: \(\left\{ \begin{gathered}{n_E} = a + b = 0,1 \hfill \\{n_{{O_2}}} = (1,5m - 1)a + (1,5n - 0,25)b = 0,26 \hfill \\{n_{{H_2}O}} = (m + 2)a + (n + 1,5)b = 0,4 \hfill \\\end{gathered} \right.\) Từ đây suy ra được a, b. Từ đó có mối quan hệ m, n. Sau đó biện luận tìm được m, n thỏa mãn Lời giải chi tiết :
Đặt số mol của CmH2m+4O4N2: a (mol) ; số mol của CnH2n+3O2N: b (mol) CmH2m+4O4N2 + (1,5m-1)O2 → mCO2 + (m+2)H2O + N2 a → (1,5m-1)a → (m+2)a mol CnH2n+3O2N + (1,5n-0,25)O2 → nCO2 + (n+1,5)H2O + N2 b → (1,5n-0,25)b → (n+1,5)b mol Ta có hệ 3 phương trình: \(\begin{gathered}\left\{ \begin{gathered}{n_E} = a + b = 0,1 \hfill \\{n_{{O_2}}} = (1,5m - 1)a + (1,5n - 0,25)b = 0,26 \hfill \\{n_{{H_2}O}} = (m + 2)a + (n + 1,5)b = 0,4 \hfill \\ \end{gathered} \right. \Rightarrow \left\{\begin{gathered}a + b = 0,1 \hfill \\1,5(ma + nb) - (a + 0,25b) = 0,26 \hfill \\ ma + nb = 0,4 - 2a - 1,5b \hfill \\ \end{gathered} \right. \hfill \\\Rightarrow \left\{ \begin{gathered} a + b = 0,1 \hfill \\4a + 2,5b = 0,34 \hfill \\ma +nb = 0,4 - 2a - 1,5b \hfill \\ \end{gathered} \right. \Rightarrow \left\{ \begin{gathered}a = 0,06 \hfill \\b = 0,04\hfill \\3m + 2n = 11 \hfill \\ \end{gathered} \right. \hfill \\ \end{gathered} \) Do m ≥ 2 và n ≥ 1 nên m = 3 và n = 1 là nghiệm duy nhất thỏa mãn => CTPT X: C3H10O4N2 và CTPT của Y: CH5O2N E + NaOH → 2 chất khí đều làm xanh quỳ tím ẩm => CTCT của X: NH3CH3COO-COONH4 ; CTCT của Y: HCOONH4 => 2 khí làm xanh quỳ tím ẩm là NH3 và CH3NH3 Muối thu được gồm: (COONa)2: 0,06 mol và HCOONa: 0,04 (mol) => a = 0,06.134 + 0,04.68=10,76 (g)
Câu 25 :
Cho dung dịch metyl amin dư lần lượt vào các dung dịch riêng biệt sau: AlCl3, FeCl3, Zn(NO3)2, Cu(NO3)2, HCl, Na2SO4. Sau khi các phản ứng kết thúc, số kết tủa thu được là
Đáp án : A Phương pháp giải :
CH3NH2 có tính chất hóa học hoàn toàn tương tự như NH3. Lời giải chi tiết :
\(\left\{ \begin{gathered}AlC{l_3} \hfill \\FeC{l_3} \hfill \\Zn{(N{O_3})_3} \hfill \\Cu{(N{O_3})_2} \hfill \\\hfill\\HCl \hfill \\N{a_2}S{O_4} \hfill \\\end{gathered} \right.\xrightarrow{{C{H_3}N{H_2}\,vua\,du}}\left| \begin{gathered}Ket\,tua\left\{ \begin{gathered}Al{(OH)_3} \hfill \\Fe{(OH)_3} \hfill \\Zn{(OH)_2} \hfill \\Cu{(OH)_2} \hfill \\\end{gathered} \right.\xrightarrow{{C{H_3}N{H_2}\,du}}\left\{ \begin{gathered}Al{(OH)_3} \hfill \\Fe{(OH)_3} \hfill \\\end{gathered} \right. \hfill \\\hfill \\C{H_3}N{H_3}Cl \hfill \\ khong\,pu \hfill \\ \end{gathered} \right.\) PTHH xảy ra: - Khi CH3NH2 vừa đủ: AlCl3 + 3CH3NH2 + 3H2O → Al(OH)3↓ + 3CH3NH3Cl FeCl3 + 3CH3NH2 + 3H2O → Fe(OH)3↓ + 3CH3NH3Cl Zn(NO3)2 + 2CH3NH2 + 2H2O → Zn(OH)2↓ + 2CH3NH3NO3 Cu(NO3)2 + 2CH3NH2 + 2 H2O → Cu(OH)2↓ + 2CH3NH3NO3 HCl + CH3NH2 → CH3NH3Cl - Khi CH3NH2 dư thì có sự hòa tan kết tủa Zn(OH)2 và Cu(OH)2 để tạo phức amin: Zn(OH)2 + 6CH3NH2 → (Zn(CH3NH2)6)(OH)2 Cu(OH)2 + 4CH3NH2 → (Cu(CH3NH2)4)(OH)2 Vậy có 2 kết tủa thu được sau phản ứng là Al(OH)3 và Fe(OH)3
Câu 26 :
Cho X, Y là hai axit cacboxylic đơn chức (MX < MY); T là este ba chức, mạch hở được tạo bởi X, Y với glixerol. Cho 23,06 gam hỗn hợp E gồm X, Y, T và glixerol (với số mol của X bằng 8 lần số mol của T) tác dụng vừa đủ với 200 ml dung dịch NaOH 2M, thu được hỗn hợp F gồm hai muối có tỉ lệ mol 1 : 3 và 3,68 gam glixerol. Đốt cháy hoàn toàn F cần vừa đủ 0,45 mol O2, thu được Na2CO3, H2O và 0,4 mol CO2. Phần trăm khối lượng của T trong E có giá trị gần nhất với giá trị nào sau đây?
Đáp án : B Phương pháp giải :
\(E\left\{ \begin{gathered}X:8x \hfill \\Y:y \hfill \\ Z:x \hfill \\glixerol:z \hfill \\\end{gathered}\right.\xrightarrow{{ + 0,4molNaOH}}\left\{ \begin{gathered}{R_1}{\text{COONa}} \hfill \\{R_2}{\text{COONa}} \hfill \\{\text{glixerol:0,4}} \hfill \\ \end{gathered} \right.\) Vì 2 muối có tỉ lệ 1 : 3 nên giả sử: R1COONa : 0,3 mol và R2COONa : 0,1 mol Đốt muối có Muối + 0,45 mol O2 → CO2 + H2O + Na2CO3 → bảo toàn O có : 2nCOO- + 2nO2 = 2nCO2 + 3nNa2CO3 + nH2O => H2O = ? mol Bảo toàn khối lượng: mmuối + mO2 = mCO2 + mNa2CO3 + mH2O => mmuối = ? (g) Mặt khác: mmuối = 0,3(R1 + 67) + 0,1.(R2 + 67) => Mối quan hệ R1, R2 => Chạy giá trị tìm được R1,R2 Bảo toàn khối lượng phản ứng tác dụng với NaOH có mE + mNaOH = mmuối + mGlixerol + mH2O => nH2O = ? →nX = ? mol và nY = ? => CTCT của Z. Từ đó tính được phần trăm =? Lời giải chi tiết :
\(E\left\{ \begin{gathered}X:8x \hfill \\Y:y \hfill \\Z:x \hfill \\glixerol:z \hfill \\ \end{gathered}\right.\xrightarrow{{ + 0,4molNaOH}}\left\{ \begin{gathered}{R_1}{\text{COONa}} \hfill \\{R_2}{\text{COONa}} \hfill \\{\text{glixerol:0,4}} \hfill \\ \end{gathered} \right.\) Vì 2 muối có tỉ lệ 1 : 3 nên giả sử: R1COONa : 0,3 mol và R2COONa : 0,1 mol Đốt muối có Muối + 0,45 mol O2 → CO2 + H2O + Na2CO3 BTNT “Na”: nNa2CO3 = 1/2n NaOH = 0,2 (mol) → bảo toàn O có : 2nCOO- + 2nO2 = 2nCO2 + 3nNa2CO3 + nH2O => H2O = 2.0,4 + 2.0,45 -2.0,4-3.0,2 = 0,3 mol Bảo toàn khối lượng: mmuối + mO2 = mCO2 + mNa2CO3 + mH2O => mmuối = 0,4.44 + 0,2.106 + 0,3.18 – 0,45.32 = 29,8 (g) Bảo toàn khối lượng có mmuối = 29,8 g = 0,3(R1 + 67) + 0,1.(R2 + 67) => 3R1 + R2 = 30 => R1 = 1 và R2 = 27 là nghiệm thỏa mãn Bảo toàn khối lượng phản ứng tác dụng với NaOH có mE + mNaOH = mmuối + mGlixerol + mH2O => 23,06 + 0,4.40 = 29,8 + 3,68 + mH2O => mH2O = 5,58 (g) => nH2O = 0,31mol → nZ = (0,4 - 0,31) : 3 = 0,03 mol →nX = 0,24 mol và nY = 0,07 → có nX + 2nZ = nR1COONa nên Z tạo từ 2X và 1 Y Z là (HCOO)2-C3H5-OOC-C2H3 : 0,03 →%Z = 26,28% gần nhất với 26%
Câu 27 :
Hỗn hợp E gồm bốn este đều có công thức C8H8O2 và có vòng benzen. Cho 16,32 gam E tác dụng tối đa với V ml dung dịch NaOH 1M (đun nóng), thu được hỗn hợp X gồm các ancol và 18,78 gam hỗn hợp muối. Cho toàn bộ X vào bình đựng kim loại Na dư, sau khi phản ứng kết thúc khối lượng chất rắn trong bình tăng 3,83 gam so với ban đầu. Giá trị của V là
Đáp án : D Phương pháp giải :
Ta thấy C8H8O2 có các đồng phân este là: HCOOCH2C6H5 C6H5COOCH3 HCOOC6H4CH3 (o,m,p) Do cho E tác dụng với NaOH thu được các ancol nên E chứa HCOOCH2C6H5, C6H5COOCH3 và 2 este còn lại đều có công thức là HCOOC6H4CH3 (o,m hoặc m,p hoặc o,p) Coi E chứa HCOOCH2C6H5 (x mol), C6H5COOCH3 (y mol), HCOOC6H4CH3 (z mol) Dựa vào các dữ kiện đề bài để lập hệ phương trình. Lời giải chi tiết :
Ta thấy C8H8O2 có các đồng phân este là: HCOOCH2C6H5 C6H5COOCH3 HCOOC6H4CH3 (o,m,p) Do cho E tác dụng với NaOH thu được các ancol nên E chứa HCOOCH2C6H5, C6H5COOCH3 và 2 este còn lại đều có công thức là HCOOC6H4CH3 (o,m hoặc m,p hoặc o,p) Coi E chứa HCOOCH2C6H5 (x mol), C6H5COOCH3 (y mol), HCOOC6H4CH3 (z mol) + nE = x + y + z = 16,32 : 136 = 0,12 mol (1) + X chứa: C6H5CH2OH (x mol) CH3OH (y mol) nH2 = 0,5x + 0,5y (mol) m bình tăng = m ancol – mH2 = 108x + 32y – 2.(0,5x+0,5y) = 3,83 (2) + Muối gồm: HCOONa (x + z mol); C6H5COONa (y mol) và CH3C6H4ONa (z mol) => m muối = 68(x+z) + 144y + 130z = 18,78 (3) Giải (1) (2) (3) được x = 0,03; y = 0,02; z = 0,07 nNaOH = x + y + 2z = 0,19 mol => V = 190ml
Câu 28 :
Cho X, Y, Z là 3 peptit mạch hở (phân tử có số nguyên tử cacbon tương ứng 8, 9, 11; Z có nhiều hơn Y một liên kết peptit); T là este no, đơn chức, mạch hở. Chia 249,56 gam hỗn hợp E gồm X, Y, Z, T thành hai phần bằng nhau. Đốt cháy hoàn toàn phần một, thu dược a mol CO2 và (a-0,11) mol H2O. Thủy phân hoàn toàn phần hai bằng dung dịch NaOH vừa đủ, thu được ancol etylic và 133,18 gam hỗn hợp G (gồm 4 muối của Gly, Ala, Val và axit cacboxylic). Đốt cháy hoàn toàn G, cần vừa đủ 3,385 mol O2. Phần trăm khối lượng của Y trong E là
Đáp án : B Phương pháp giải :
\(\left\{ \begin{gathered}X(8C) \hfill \\Y(9C) \hfill \\Z(11C) \hfill \\T:{C_n}{H_{2n}}{O_2} \hfill \\\end{gathered} \right.\xrightarrow{{quy\,doi}}\underbrace {\left\{ \begin{gathered}C{H_2}:x \hfill \\CONH:y \hfill \\{H_2}O:z \hfill \\{O_2}:T \hfill \\ \end{gathered} \right.}_{249,56(g)}\) Áp dụng các định luật bảo toàn khối lượng, bảo toàn nguyên tố để lập nên các phương trình. Lời giải chi tiết :
\(\begin{gathered} \left\{ \begin{gathered}X(8C) \hfill \\Y(9C) \hfill \\Z(11C) \hfill \\T:{C_n}{H_{2n}}{O_2}\hfill \\\end{gathered} \right.\xrightarrow{{quy\,doi}}\underbrace {\left\{\begin{gathered}C{H_2}:x \hfill \\CONH:y \hfill \\{H_2}O:z \hfill \\{O_2}:T \hfill \\ \end{gathered} \right.}_{249,56(g)}\left| \begin{gathered}P1\xrightarrow{{ + {O_2}}}\left\{ \begin{gathered}C{O_2}:amol \hfill \\{H_2}O:a - 0,11\,mol \hfill \\ \end{gathered} \right. \hfill \\P2\xrightarrow{{ + NaOH:(y + t)\,mol}}{H_2}O:z\,mol + \,{C_2}{H_5}OH:t\,mol + G\left\{ \begin{gathered}{C_n}{H_{2n}}{O_2}NNa \hfill \\{C_m}{H_{2m - 1}}{O_2}Na \hfill \\ \end{gathered} \right. \hfill \\ \end{gathered} \right. \hfill \\G\left\{ \begin{gathered}{C_n}{H_{2n}}{O_2}NNa \hfill \\{C_m}{H_{2m - 1}}{O_2}Na \hfill \\ \end{gathered} \right.\xrightarrow{{ + {O_2}:3,385mol}}\left\{ \begin{gathered}N{a_2}C{O_3}:0,5y + 0,5t \hfill \\C{O_2}:a + 0,5y - 2,5t \hfill \\{H_2}O:x + y - 2,5t \hfill \\\end{gathered} \right. \hfill \\ \end{gathered} \) P1: nCO2 –nH2O = 0,11 => 0,5y – z = 0,11 (1) P2: nNaOH = y + t => nNa2CO3 = 0,5y + 0,5t BT “C”: x + y -2t = 0,5y + 0,5t + nCO2 => nCO2 = x + 0,5y – 2,5t BT “H”: (2x + y + 2z)+(y + t) -2z - 6t = 2nH2O => nH2O = x + y – 2,5t BT “O”: nO(muối) + 3,385.2 = 3(0,5y + 0,5t) + 2(x + 0,5y – 2,5t) + (x + y – 2,5t) => 3x + 1,5y – 8t = 6,77 (2) Phương trình về KL: 14x + 43y + 18z + 32t = 249,56:2 (3) BTKL: 124,78 + 4(y+t) = 133,18 + 18z + 46t => 40y – 18z – 6t = 8,4 (4) (1) (2) (3) (4) => x = 4,98; y = 0,42; z = 0,1; t = 1,1 \(\begin{gathered}\left\{ \begin{gathered}{n_{peptit}} = 0,1{\text{ }}mol \to 0,8 < n < 1,1 \hfill \\{n_{C(hh)}} = 4,98 + 0,42 = 5,4 \hfill \\ \end{gathered} \right. \to 4,3 < {n_{C(este)}} < 4,6 \to \frac{{4,3}}{{1,1}} < C(este) <\frac{{4,6}}{{1,1}} \hfill \\ \to Este:{C_4}{H_8}{O_2} \hfill \\\to \left\{ \begin{gathered}{n_{C(peptit)}} = 5,4- 4,4 = 1 \hfill \\{n_{peptit}} = z = 0,1 \hfill \\{n_{CONH}} = 0,42 \to so\,mat\,xich\,tb = 4,2 \hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}Z:Gl{y_4}Ala(m) \hfill \\Y:Gl{y_3}Ala(n) \hfill \\X:ValAla(p)\hfill \\ \end{gathered} \right. \to \left\{ \begin{gathered}m + n + p = 0,1 \hfill \\11m + 9n + 8p = 1 \hfill \\5m + 4n + 2p = 0,42 \hfill \\\end{gathered} \right. \to \left\{ \begin{gathered}m = 0,06 \hfill \\n = 0,02 \hfill \\z = 0,02 \hfill \\\end{gathered} \right. \hfill \\\to \% {m_Y} = \frac{{0,02.(75.3 + 89 - 18.3)}}{{124,78}}.100\% = 4,17\% \hfill \\\end{gathered} \)
Câu 29 :
Poli(metyl metacrylat) và nilon-6 được tạo thành từ các monome tương ứng là
Đáp án : B Phương pháp giải :
Từ tên của polime ta suy ra được các monome tương ứng Lời giải chi tiết :
\(\begin{gathered}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3} \hfill \\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,| \hfill \\nC{H_2} = C(C{H_3}) - COOC{H_3}\xrightarrow{{{t^o},xt,p}}{{\text{(}}C{H_2} - C - {\text{)}}_n} \hfill \\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,| \hfill \\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,COOC{H_3} \hfill \\(Metyl\,metacrylat)\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,Poli(metyl\,metacrylat) \hfill \\ \end{gathered} \) Phản ứng trùng ngưng tạo nilon-6: \(n{H_2}N - {{\text{(}}C{H_2})_5} - C{\text{OO}}H\xrightarrow{{{t^o},p,xt}}{( - HN - {{\text{(}}C{H_2})_5} - C{\text{O}} - )_n} + n{H_2}O\) (Axit ε-aminocaproic) (Tơ nilon-6)
Câu 30 :
Este X có công thức phân tử C6H10O4. Xà phòng hóa hoàn toàn X bằng dung dịch NaOH, thu được ba chất hữu cơ Y, Z, T. Biết Y tác dụng với Cu(OH)2 tạo dung dịch màu xanh lam. Nung nóng Z với hỗn hợp rắn gồm NaOH và CaO, thu được CH4. Phát biều nào sau đây sai?
Đáp án : B Phương pháp giải :
- Độ bất bão hòa của X: k = (2C + 2 -H)/2 = (2.6 + 2 - 10)/2 = 2 => Este X là este no, 2 chức - Y phản ứng với Cu(OH)2 tạo dung dịch xanh lam nên Y là ancol 2 chức chứa 2 nhóm OH cạnh nhau - Nung nóng Z với hỗn hợp rắn gồm NaOH và CaO, thu được CH4 => Z Dựa vào các dữ kiện đề bài để tìm CTCT phù hợp của các chất. Lời giải chi tiết :
- Độ bất bão hòa của X: k = (2C + 2 -H)/2 = (2.6 + 2 - 10)/2 = 2 => Este X là este no, 2 chức - Y phản ứng với Cu(OH)2 tạo dung dịch xanh lam nên Y là ancol 2 chức chứa 2 nhóm OH cạnh nhau - Z là CH3COONa vì: CH3COONa + NaOH \(\xrightarrow{{CaO,{t^o}}}\) CH4 + Na2CO3 Vậy có thể suy ra công thức cấu tạo thỏa mãn của este X là: CH3COOCH(CH3)-CH2-OOCH hoặc CH3COOCH2-CH(CH3)-OOCH => T là HCOONa, Y là CH3-CH(OH)-CH2(OH) A, C, D đúng B sai vì Y có mạch C không phân nhánh
Câu 31 :
Khi nghiên cứu cacbohidrat X ta nhận thấy: - X không tráng gương, có một đồng phân - X thủy phân trong nước được hai sản phẩm. Vậy X là
Đáp án : C Phương pháp giải :
Dựa vào tính chất hóa học của cacbohidrat. Lời giải chi tiết :
Xét các phương án ta thấy chỉ có saccarozo thỏa mãn vì: - Saccarozo không tráng gương, có 1 đồng phân là mantozo - Saccarozo thủy phân trong nước thu được 2 sản phẩm là glucozo và fructozo
Câu 32 :
Cho các phát biểu sau: (a) Sau khi mổ cá, có thể dùng chanh để giảm mùi tanh. (b) Dầu thực vật và dầu nhớt bôi trơn máy đều có thành phần chính là chất béo. (c) Cao su thiên nhiên là polime của isopren. (d) Khi làm trứng muối (ngâm trứng trong dung dịch NaCl bão hòa) xảy ra hiện tượng đông tụ protein. (e) Thành phần chính của tóc là protein. (g) Để giảm đau nhức khi bị kiến đốt, có thể bôi giấm vào vết đốt. Số phát biểu đúng là
Đáp án : B Lời giải chi tiết :
(a) đúng vì các amin sẽ phản ứng với chanh tạo muối và bị rửa trôi (b) sai vì dầu nhớt bôi trơn có thành phần chính là các hidrocacbon (c) đúng (d) đúng vì protein bị đông tụ khi đun nóng hoặc khi tiếp xúc với một số muối. (e) đúng (g) sai vì nọc kiến có chứa HCOOH nên bôi giấm (CH3COOH) không có tác dụng, ta nên bôi nước vôi trong Ca(OH)2 để giảm sưng tấy. Vậy có tất cả 4 phát biểu đúng
Câu 33 :
Cho 0,1 mol chất X có công thức là C2H12O4N2S tác dụng với dung dịch chứa 0,35 mol NaOH đun nóng thu được chất khí làm xanh giấy quỳ ẩm và dung dịch Y. Cô cạn dung dịch Y, thu được m gam chất rắn khan. Giá trị của m là
Đáp án : B Phương pháp giải :
X tác dụng NaOH đun nóng thu được chất khí làm xanh giấy quỳ tím ẩm nên ta suy ra cấu tạo phù hợp của X là: (CH3NH3)2SO4 Tính toán theo PTHH suy ra giá trị của m. Lời giải chi tiết :
X tác dụng NaOH đun nóng thu được chất khí làm xanh giấy quỳ tím ẩm nên ta suy ra cấu tạo phù hợp của X là: (CH3NH3)2SO4 PTHH: (CH3NH3)2SO4 + 2NaOH → Na2SO4 + 2CH3NH2 + 2H2O ĐB: 0,1 mol 0,35 mol PƯ: 0,1 mol → 0,2 mol → 0,1 mol Sau: 0 0,15 mol 0,1 mol Vậy chất rắn thu được gồm NaOH dư (0,15 mol) và Na2SO4 (0,1 mol) => m = 0,15.40 + 0,1.142 = 20,2 gam
Câu 34 :
Cho hỗn hợp E gồm 0,1 mol X (C5H11O4N) và 0,15 mol Y (C5H14O4N2, là muối của axit cacboxylic hai chức) tác dụng hoàn toàn với dung dịch KOH, thu được một ancol đơn chức, hai amin no (kế tiếp trong dãy đồng đẳng) và dung dịch T. Cô cạn T, thu được hỗn hợp G gồm ba muối khan có cùng số nguyên tử cacbon trong phân tử (trong đó có hai muối của hai axit cacboxylic và muối của một α-amino axit). Phần trăm khối lượng của muối có phân tử khối lớn nhất trong G là
Đáp án : C Phương pháp giải :
Do thu được 2 amin no kế tiếp nhau trong dãy đồng đẳng nên suy ra Y là C2H5NH3OOC-COONH3CH3 => Muối có 2C => ancol có 1C => CTCT của X Lời giải chi tiết :
Do thu được 2 amin no kế tiếp nhau trong dãy đồng đẳng nên suy ra Y là C2H5NH3OOC-COONH3CH3 => Muối có 2C => ancol có 1C => X là CH3COONH3-CH2-COOCH3 Vậy muối G gồm: KOOC-COOK (0,15 mol) H2N-CH2-COOK (0,1 mol) CH3-COOK (0,1 mol) %m KOOC-COOK = \(\frac{{0,15.166}}{{0,15.166 + 0,1.113 + 0,1.98}}.100\% \) = 54,13%
Câu 35 :
Thủy phân hoàn toàn a gam triglixerit X trong dung dịch NaOH, thu được glixerol và dung dịch chứa m gam hỗn hợp muối (gồm natri stearat; natri panmitat và C17HyCOONa). Đốt cháy hoàn toàn a gam X cần 1,55 mol O2, thu được H2O và 1,1 mol CO2. Giá trị của m là
Đáp án : D Phương pháp giải :
Do muối gồm natri stearat (C17H35COONa); natri panmitat (C15H31COONa) và C17HyCOONa nên X số nguyên tử C là: 18 + 16 + 18 + 3 = 55 => nX = nCO2 : 55 = ? Do X chứa 6 nguyên tử O nên: nO(X) = 6nX = ? *Xét phản ứng cháy của X: BTNT "O": nO(X) + 2nO2 = 2nCO2 + nH2O => nH2O BTKL: mX = mCO2 + mH2O - mO2 *Xét phản ứng thủy phân X trong NaOH: X + 3NaOH → Muối + C3H5(OH)3 BTKL: m muối = mX + mNaOH - mC3H5(OH)3 Lời giải chi tiết :
Do muối gồm natri stearat (C17H35COONa); natri panmitat (C15H31COONa) và C17HyCOONa nên X số nguyên tử C là: 18 + 16 + 18 + 3 = 55 => nX = nCO2 : 55 = 1,1 : 55 = 0,02 mol Do X chứa 6 nguyên tử O nên: nO(X) = 6nX = 6.0,02 = 0,12 mol *Xét phản ứng cháy của X: BTNT "O": nO(X) + 2nO2 = 2nCO2 + nH2O => 0,12 + 2.1,55 = 2.1,1 + nH2O => nH2O = 1,02 mol BTKL: mX = mCO2 + mH2O - mO2 = 1,1.44 + 1,02.18 - 1,55.32 = 17,16 gam *Xét phản ứng thủy phân X trong NaOH: X + 3NaOH → Muối + C3H5(OH)3 0,02 → 0,06 → 0,02 BTKL: m muối = mX + mNaOH - mC3H5(OH)3 = 17,16 + 0,06.40 - 0,02.92 = 17,72 gam
Câu 36 :
Cho sơ đồ chuyển hóa sau: (1) n-pentan \(\xrightarrow{{{t^o}}}\) A + B và D + E (2) A + Cl2 \(\xrightarrow{{a/s}}\) CH3-CHCl-CH3 + F (3) CH3COONa + NaOH → D + G (4) D + Cl2 \(\xrightarrow{{a/s}}\) L + F (5) CH3-CHCl-CH3 + L + Na → M + NaCl Các chất A, B, D, E và M lần lượt có cấu tạo là
Đáp án : C Phương pháp giải :
Xem lại lý thuyết về hidrocacbon Lời giải chi tiết :
3) CH3COONa + NaOH \(\xrightarrow{{CaO,{t^o}}}\) CH4 (D) + Na2CO3 (G) (4) CH4 (D) + Cl2 \(\xrightarrow{{a/s}}\) CH3Cl (L) + HCl (F) (1) CH3-CH2-CH2-CH2-CH3 \(\xrightarrow{{crackinh}}\) CH4 (D) + CH2=CH-CH2-CH3 (E) CH3-CH2-CH2-CH2-CH3 \(\xrightarrow{{crackinh}}\) CH3-CH2-CH3 (A) + CH2=CH2 (B) (2) CH3-CH2-CH3 (A) + Cl2 \(\xrightarrow{{a/s}}\) CH3-CHCl-CH3 + HCl (F) (5) CH3-CHCl-CH3 + CH3Cl (L) + 2Na → CH3-CH(CH3)-CH3 (M) + 2NaCl
Câu 37 :
Hỗn hợp E gồm ba este mạch hở, đều có bốn liên kết π trong phân tử, trong đó có một este đơn chức là este của axit metacrylic và hai este hai chức là đồng phân của nhau. Đốt cháy hoàn toàn 12,22 gam E bằng O2, thu được 0,37 mol H2O. Mặt khác, cho 0,36 mol E phản ứng vừa đủ với 234 ml dung dịch NaOH 2,5M, thu được hỗn hợp X gồm các muối của các axit cacboxylic không no, có cùng số nguyên tử cacbon trong phân tử; hai ancol không no, đơn chức có khối lượng m1 gam và một ancol no, đơn chức có khối lượng m2 gam. Tỉ lệ m1 : m2 có giá trị gần nhất với giá trị nào sau đây?
Đáp án : C Phương pháp giải :
Bảo toàn nguyên tố Lời giải chi tiết :
nNaOH = 0,234.2,5 = 0,585 mol *Xét phản ứng thủy phân hỗn hợp E trong NaOH: Đặt n este đơn chức = x và n este hai chức = y (mol) => nE = x + y = 0,36 mol và nNaOH = x + 2y = 0,585 Giải hệ thu được x = 0,135 và y = 0,225 => x : y = 3 : 5 *Xét phản ứng đốt cháy E: Do X, Y đều chứa 4 liên kết π nên ta giả sử E gồm: CnH2n-6O2 (3a mol) và CmH2m-6O4 (5a mol) nCO2 - nH2O = 3nE => nCO2 - 0,37 = 3.8a => nCO2 = 24a + 0,37 (mol) Mặt khác: mE = mC + mH + mO => 12(24a + 0,37) + 0,37.2 + 3a.32 + 5a.64 = 12,22 => a = 0,01 mol => nCO2 = 24.0,01 + 0,37 = 0,61 mol; n este đơn chức = 0,03 và n este hai chức = 0,05 (mol) BTNT "C": nCO2 = 0,03n + 0,05m = 0,61 chỉ có nghiệm n = 7 và m = 8 thỏa mãn (Do các axit đều 4C và ancol không no tối thiểu 3C nên n≥7 và m≥8) Do thủy phân E trong NaOH thu được hỗn hợp X gồm các muối của các axit cacboxylic không no, có cùng số nguyên tử cacbon trong phân tử; hai ancol không no, đơn chức và một ancol no, đơn chức nên ta suy ra cấu tạo của các chất trong E là: X: CH2=C(CH3)-COOCH2-C≡CH (0,03 mol) Y: CH3-OOC-CH=CH-COO-CH2-CH=CH2 COO-CH2-CH=CH2 Z: C=C COO-CH3 Ancol đa chức gồm: CH≡C-CH2-OH (0,03 mol) và CH2=CH-CH2-OH (0,05 mol) => m1 = 0,03.56 + 0,05.58 = 4,58 gam Ancol đơn chức gồm: CH3OH (0,05 mol) => m2 = 0,05.32 = 1,6 gam => m1 : m2 = 4,58 : 1,6 = 2,8625 gần nhất với 2,9
Câu 38 :
Hỗn hợp X gồm alanin, axit glutamic và axit acrylic. Hỗn hợp Y gồm propen và trimetylamin. Đốt cháy hoàn toàn a mol X và b mol Y thì tổng số mol oxi cần dùng vừa đủ là 1,14 mol, thu được H2O, 0,1 mol N2 và 0,91 mol CO2. Mặt khác, khi cho a mol X tác dụng với dung dịch KOH dư thì lượng KOH phản ứng là m gam. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Đáp án : D Phương pháp giải :
Alanin: CH3-CH(NH2)-COOH ↔ (CH2)2(COO)(NH3) Axit glutamic: HOOC-CH2-CH2-CH(NH2)-COOH ↔ (COO)2(CH2)3(NH3) Axit acrylic: CH2=CH-COOH ↔ (CH2)2(COO) Propen: C3H6 ↔ (CH2)3 Trimetylamin: (CH3)3N ↔ (CH2)3(NH3) Vậy quy đổi hỗn hợp X, Y thành CH2 (x mol), COO(y mol), NH3 (với nNH3 = 2nN2) Dựa vào phương pháp bảo toàn nguyên tố C và O tìm được giá trị của x, y Lời giải chi tiết :
Alanin: CH3-CH(NH2)-COOH ↔ (CH2)2(COO)(NH3) Axit glutamic: HOOC-CH2-CH2-CH(NH2)-COOH ↔ (COO)2(CH2)3(NH3) Axit acrylic: CH2=CH-COOH ↔ (CH2)2(COO) Propen: C3H6 ↔ (CH2)3 Trimetylamin: (CH3)3N ↔ (CH2)3(NH3) Vậy quy đổi hỗn hợp X, Y thành CH2 (x mol), COO(y mol), NH3 (với nNH3 = 2nN2 = 0,2 mol) \(\left\{ \begin{gathered}C{H_2}:x \hfill \\{\text{COO:y}} \hfill \\{\text{N}}{{\text{H}}_{\text{3}}}{\text{:0,2}} \hfill \\ \end{gathered} \right. + {O_2}:1,14 \to \left\{ \begin{gathered}C{O_2}:0,91 \hfill \\\xrightarrow{{BT:H}}{H_2}O:x + 0,3 \hfill \\{N_2}:0,1 \hfill \\ \end{gathered} \right.\) BTNT "C": nCH2 + nCOO = nCO2 => x + y = 0,91 (1) BTNT "O": 2nCOO + 2nO2 = 2nCO2 + nH2O => 2y + 1,14.2 = 0,91.2 + x + 0,3 (2) Giải hệ được x = 0,66 và y = 0,25 Khi cho a mol X tác dụng với KOH thì: nKOH = nCOO = 0,25 mol => mKOH = 0,25.56 = 14 gam
Câu 39 :
Cho các phát biểu sau: (a) Đipeptit Val-Lys có phản ứng màu biure. (b) Dung dịch axit glutamic đổi màu quỳ tím thành xanh. (c) Etyl fomat và glucozo có cùng công thức đơn giản nhất. (d) Phenylamin có lực bazo mạnh hơn amoniac. (e) Saccarozo có phản ứng thủy phân trong môi trường axit. (g) Vinyl axetat làm mất màu dung dịch brom. Số phát biểu đúng là
Đáp án : C Lời giải chi tiết :
(a) sai vì đipeptit không có phản ứng màu biure (b) sai vì axit glutamic làm quỳ tím chuyển thành đỏ (c) sai vì: + Etyl fomat (CTCT: HCOOC2H5; CTPT: C3H6O2) có CTĐGN là C3H6O2 + Glucozo (CTPT: C6H12O6) có CTĐGN là CH2O (d) sai vì tính bazo của phenylamin yếu hơn amoniac (e) đúng, saccarozo thủy phân trong môi trường axit khi đun nóng thu được glucozo và fructozo (g) đúng vì phân tử vinyl axetat (CH3COOCH=CH2) có chứa liên kết đôi C=C Vậy có tất cả 2 phát biểu đúng.
Câu 40 :
Cho các phát biểu sau: (a) Thủy phân triolein, thu được etylen glicol. (b) Tinh bột bị thủy phân khi có xúc tác axit hoặc enzim. (c) Thủy phân vinyl fomat, thu được hai sản phẩm đều có phản ứng tráng bạc. (d) Trùng ngưng ε-aminocaproic, thu được policaproamit. (e) Chỉ dùng quỳ tím có thể phân biệt ba dung dịch: alanin, lysin, axit glutamic. (f) Phenylamin tan ít trong nước nhưng tan tốt trong dung dịch HCl. Số phát biểu đúng là
Đáp án : C Lời giải chi tiết :
(a) sai vì thủy phân triolein (là một loại chất béo) thu được glixerol (b) đúng, khi có mặt xúc tác axit hoặc enzim thì tinh bột bị thủy phân thành glucozo (c) đúng + Khi thủy phân trong môi trường axit: HCOOCH=CH2 + H2O \(\xrightarrow{{{H^ + },{t^o}}}\) HCOOH + CH3CHO Cả HCOOH và CH3CHO đều có phản ứng tráng gương + Khi thủy phân trong môi trường kiềm: HCOOCH=CH2 + NaOH \(\xrightarrow{{{t^o}}}\) HCOONa + CH3CHO Cả HCOONa và CH3CHO đều có phản ứng tráng gương (d) đúng \(n{H_2}N - {{\text{(}}C{H_2})_5} - C{\text{OO}}H\xrightarrow{{{t^o},p,xt}}{( - HN - {{\text{(}}C{H_2})_5} - C{\text{O}} - )_n} + n{H_2}O\) (Axit ε-aminocaproic) (Policaproamit) (e) đúng, vì alanin không làm quỳ tím chuyển màu; lysin làm quỳ tím chuyển xanh; axit glutamic làm quỳ tím chuyển đỏ (f) đúng Vậy có tất cả 5 phát biểu đúng |