Đề thi giữa kì 2 Hóa 8 - Đề số 1Đề bài
Câu 1 :
Cho phản ứng sau, xác định chất khử: Fe2O3 + 3H2 $\xrightarrow{{{t}^{o}}}$ 2Fe + 3H2O
Câu 2 :
Cần bao nhiêu gam oxi để đốt cháy hết 2 mol lưu huỳnh?
Câu 3 :
Cho phản ứng: C + O2 $\xrightarrow{{{t}^{o}}}$ CO2. Phản ứng trên là:
Câu 4 :
Thành phần theo thể tích của khí nitơ, oxi, các khí khác trong không khí lần lượt là:
Câu 5 :
Cho các công thức oxit sau: CaO, CuO, NaO, CO2, CO3. Công thức oxit viết sai là
Câu 6 :
Điều chế hiđro trong công nghiệp, người ta dùng:
Câu 7 :
Sự oxi hóa có tỏa nhiệt nhưng không phát sáng được gọi là
Câu 8 :
Trong những oxit sau: CuO, MgO, Fe2O3, CaO, Na2O. Oxit nào không bị hiđro khử?
Câu 9 :
Al2O3 có bazơ tương ứng là
Câu 10 :
Chọn định nghĩa phản ứng phân hủy đầy đủ nhất:
Câu 11 :
Hợp chất nào sau đây không phải là oxit?
Câu 12 :
Cho biết phát biểu nào dưới đây là đúng:
Câu 13 :
Nhận xét nào sau đây là đúng nhất về khí hiđrô:
Câu 14 :
Công thức của bạc clorua là:
Câu 15 :
Khi đưa que đóm tàn đỏ vào miệng ống nghiệm chứa khí ôxi có hiện tượng gì xảy ra ?
Câu 16 :
Trong số những chất có công thức hoá học dưới đây, chất nào có khả năng làm cho quì tím đổi màu đỏ?
Câu 17 :
Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì?
Câu 18 :
Đốt cháy 7,8 gam khí axetilen (C2H2) trong khí oxi, thu được 11,2 lít khí CO2 (đktc) và m2 gam H2O. Giá trị m2 là
Câu 19 :
Đốt 9 kg than đá chứa 20% tạp chất. Tính thể tích khí cacbonic sinh ra ở đktc. (Giải thích: Than đá chứa thành phần chính là cacbon C, mà than đá chứa 20% tạp chất thì %C = 100 – 20 = 80%).
Câu 20 :
Nhiệt phân cùng một lượng số mol mỗi chất sau: KMnO4; KClO3; KNO3; H2O2. Chất nào thu được lượng khí oxi lớn nhất?
Câu 21 :
Thể tích không khí ( ở đktc) cần dùng để đốt cháy hết 1,2 kg C là? Biết oxi chiếm 20% thể tích không khí
Câu 22 :
Khử hoàn toàn sắt (II) oxit bằng a(g) khí H2 thu được 5,6 gam sắt. Giá trị của a là:
Câu 23 :
Cho 6,5 gam Zn phản ứng với axit clohiđric (HCl) thấy có khí bay lên với thể tích là
Câu 24 :
Cho mẩu Na vào cốc nước dư thấy có 4,48 lít khí bay lên ở đktc. Tính khối lượng Na phản ứng
Câu 25 :
Cho 0,1 mol NaOH tác dụng với 0,2 mol HCl, sản phẩm sinh ra sau phản ứng là muối NaCl và nước. Khối lượng muối NaCl thu được là
Lời giải và đáp án
Câu 1 :
Cho phản ứng sau, xác định chất khử: Fe2O3 + 3H2 $\xrightarrow{{{t}^{o}}}$ 2Fe + 3H2O
Đáp án : B Phương pháp giải :
Chất khử là chất lấy oxi của chất khác. Lời giải chi tiết :
Chất khử là chất lấy oxi của chất khác. Trong phản ứng này, H2 là chất lấy oxi của Fe2O3 => H2 là chất khử
Câu 2 :
Cần bao nhiêu gam oxi để đốt cháy hết 2 mol lưu huỳnh?
Đáp án : C Phương pháp giải :
PTHH: S + O2 $\xrightarrow{{{t}^{o}}}$ SO2 +) Tính số mol O2 theo S
Lời giải chi tiết :
PTHH: S + O2 $\xrightarrow{{{t}^{o}}}$ SO2 Tỉ lệ PT: 1mol 1mol Phản ứng: 2mol → 2mol => Khối lượng oxi cần dùng là: ${{m}_{{{O}_{2}}}}=n.M=2.32=64\,gam$
Câu 3 :
Cho phản ứng: C + O2 $\xrightarrow{{{t}^{o}}}$ CO2. Phản ứng trên là:
Đáp án : D Phương pháp giải :
Phản ứng hóa hợp là phản ứng hóa học trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu. Lời giải chi tiết :
Phản ứng đốt cháy cacbon (than) trong khí oxi: C + O2 $\xrightarrow{{{t}^{o}}}$ CO2 Ta thấy: chất mới CO2 được tạo thành từ 2 chất ban đầu là C và O2 => đây là phản ứng hóa hợp. Vì C phản ứng với O2 tỏa nhiều nhiệt => đây là phản ứng cháy, tỏa nhiệt.
Câu 4 :
Thành phần theo thể tích của khí nitơ, oxi, các khí khác trong không khí lần lượt là:
Đáp án : B Lời giải chi tiết :
Thành phần theo thể tích của khí nitơ, oxi, các khí khác trong không khí lần lượt là: 78%, 21%, 1%
Câu 5 :
Cho các công thức oxit sau: CaO, CuO, NaO, CO2, CO3. Công thức oxit viết sai là
Đáp án : C Lời giải chi tiết :
Ca có hóa trị II => hợp chất oxit của Ca là : CaO Cu có hóa trị II => oxit của Cu là CuO Na có hóa trị I => oxit của Na là Na2O C có hóa trị II, IV => 2 oxit của C là CO và CO2 => không có công thức oxit NaO và CO3
Câu 6 :
Điều chế hiđro trong công nghiệp, người ta dùng:
Đáp án : C Lời giải chi tiết :
Điều chế hiđro trong công nghiệp, người ta dùng phương pháp điện phân nước
Câu 7 :
Sự oxi hóa có tỏa nhiệt nhưng không phát sáng được gọi là
Đáp án : B Lời giải chi tiết :
Sự oxi hóa có tỏa nhiệt nhưng không phát sáng được gọi là sự oxi hóa chậm.
Câu 8 :
Trong những oxit sau: CuO, MgO, Fe2O3, CaO, Na2O. Oxit nào không bị hiđro khử?
Đáp án : D Lời giải chi tiết :
Những oxit không bị hiđro khử là: CaO, Na2O, MgO
Câu 9 :
Al2O3 có bazơ tương ứng là
Đáp án : D Phương pháp giải :
Oxit bazơ và bazơ tương ứng có cùng hóa trị của nguyên tố kim loại
Lời giải chi tiết :
Al2O3 có bazơ tương ứng là Al(OH)3
Câu 10 :
Chọn định nghĩa phản ứng phân hủy đầy đủ nhất:
Đáp án : C Lời giải chi tiết :
Phản ứng phân hủy là phản ứng hóa học trong đó một chất phản ứng sinh ra hai hay nhiều chất mới
Câu 11 :
Hợp chất nào sau đây không phải là oxit?
Đáp án : D Lời giải chi tiết :
Hợp chất không phải là oxit là: CuS vì không có nguyên tử O
Câu 12 :
Cho biết phát biểu nào dưới đây là đúng:
Đáp án : D Lời giải chi tiết :
A sai vì gốc sunfat SO4 hoá trị II B sai vì gốc photphat PO4 hoá trị III C sai vì gốc nitrat NO3 hoá trị I D đúng, nhóm hiđroxit OH hoá trị I
Câu 13 :
Nhận xét nào sau đây là đúng nhất về khí hiđrô:
Đáp án : D Lời giải chi tiết :
Tất cá các đáp án A, B, C đều đúng.
Câu 14 :
Công thức của bạc clorua là:
Đáp án : D Lời giải chi tiết :
Tên muối = Tên KL (kèm theo hoá trị nếu KL có nhiều hoá trị) + tên gốc axit => Công thức hóa học của bạc clorua là AgCl
Câu 15 :
Khi đưa que đóm tàn đỏ vào miệng ống nghiệm chứa khí ôxi có hiện tượng gì xảy ra ?
Đáp án : D Phương pháp giải :
Dựa vào dấu hiệu hiện tượng nhận biết ra khí oxi. Lời giải chi tiết :
Khi đưa que đóm tàn đỏ vào miệng ống nghiệm chứa khí ôxi thì tàn đóm bùng cháy.
Câu 16 :
Trong số những chất có công thức hoá học dưới đây, chất nào có khả năng làm cho quì tím đổi màu đỏ?
Đáp án : A Phương pháp giải :
Dung dịch axit làm quỳ chuyển đỏ
Lời giải chi tiết :
Dung dịch axit làm quỳ chuyển đỏ => HNO3 là chất có khả năng làm qùy chuyển đỏ
Câu 17 :
Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu gì?
Đáp án : A Lời giải chi tiết :
Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu đỏ
Câu 18 :
Đốt cháy 7,8 gam khí axetilen (C2H2) trong khí oxi, thu được 11,2 lít khí CO2 (đktc) và m2 gam H2O. Giá trị m2 là
Đáp án : C Phương pháp giải :
+) Tính số mol khí CO2 +) Vì đầu bài cho 2 số liệu số mol của chất phản ứng C2H2 và chất sản phẩm CO2 => tính toán theo chất sản phẩm +) Viết PTHH và tính số mol H2O theo CO2 Lời giải chi tiết :
Số mol khí C2H2 là: ${{n}_{{{C}_{2}}{{H}_{2}}}}=\frac{7,8}{12.2+2}=0,3\,mol$ Số mol khí CO2 là: ${{n}_{C{{O}_{2}}}}=\frac{11,2}{22,4}=0,5\,mol$ Vì đầu bài cho 2 số liệu số mol của chất phản ứng C2H2 và chất sản phẩm CO2 => tính toán theo chất sản phẩm
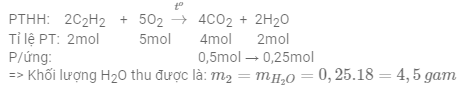
Câu 19 :
Đốt 9 kg than đá chứa 20% tạp chất. Tính thể tích khí cacbonic sinh ra ở đktc. (Giải thích: Than đá chứa thành phần chính là cacbon C, mà than đá chứa 20% tạp chất thì %C = 100 – 20 = 80%).
Đáp án : A Lời giải chi tiết :
Khối lượng C có trong than là: \({m_C} = \frac{{\% {m_C}}}{{100\% }}.{m_{than}} = \frac{{80\% }}{{100\% }}.9 = 7,2\,(kg) = 7200(g)\) Số mol C là: \({n_C} = \frac{{{m_C}}}{{{M_C}}} = \frac{{7200}}{{12}} = 600\,(mol)\) PTHH: C + O2 \(\buildrel {{t^0}} \over\longrightarrow \) CO2 Theo PTHH 1 → 1 (mol) Vậy 600 → 600 (mol) Thể tích khí CO2 (đktc) thoát ra là: VCO2(dktc) = nCO2 × 22,4 = 600×22,4 = 13440 (lít)
Câu 20 :
Nhiệt phân cùng một lượng số mol mỗi chất sau: KMnO4; KClO3; KNO3; H2O2. Chất nào thu được lượng khí oxi lớn nhất?
Đáp án : B Phương pháp giải :
+) Giả sử lấy 1 mol mỗi chất +) Viết PTHH của mỗi phản ứng nhiệt phân và tính số mol O2 theo PT
Lời giải chi tiết :
Giả sử lấy 1 mol mỗi chất Phương trình hóa học nhiệt phân: 2KMnO4 $\xrightarrow{{{t}^{o}}}$ K2MnO4 + MnO2 + O2 Tỉ lệ PT: 2mol 1mol P/ứng: 1mol → 0,5mol 2KClO3 $\xrightarrow{{{t}^{o}}}$ 2KCl + 3O2 Tỉ lệ PT: 2mol 3mol P/ứng: 1mol → 1,5mol 2KNO3 $\xrightarrow{{{t}^{o}}}$ 2KNO2 + O2 Tỉ lệ PT: 2mol 1mol P/ứng: 1mol → 0,5mol 2H2O2 $\xrightarrow{{{t}^{o}}}$ 2H2O + O2 Tỉ lệ PT: 2mol 1mol P/ứng: 1mol → 0,5mol => chất thu được lượng khí oxi lớn nhất là KClO3
Câu 21 :
Thể tích không khí ( ở đktc) cần dùng để đốt cháy hết 1,2 kg C là? Biết oxi chiếm 20% thể tích không khí
Đáp án : B Phương pháp giải :
+ Tính số mol của C + Viết PTHH xảy ra : C + O2 \(\xrightarrow{{{t^0}}}\) CO2 + Tính số mol O2 theo số mol của C + Tính thể tích không khí = 5VO2 Lời giải chi tiết :
1,2 kg = 1200 (g) Số mol cacbon là: nC = mC : MC = 1200 : 12 = 100 (mol) C + O2 \(\xrightarrow{{{t^0}}}\) CO2 100→ 100 (mol) => VO2 = 100.22, 4= 2240 (lít) \( = > {V_{kk}} = \frac{{{V_{{O_2}}}.100\% }}{{20\% }} = \frac{{2240.100\% }}{{20\% }} = 11200\,(lit)\)
Câu 22 :
Khử hoàn toàn sắt (II) oxit bằng a(g) khí H2 thu được 5,6 gam sắt. Giá trị của a là:
Đáp án : B Lời giải chi tiết :
\(FeO{\text{ }} + {\text{ }}{H_2}\xrightarrow{{{t^0}}}Fe{\text{ }} + {\text{ }}{H_2}O\) nFe = mFe : MFe =5,6 :56 = 0,1 mol Theo PTHH: nH2 = nFe = 0,1 mol => mH2 =nH2 × MH2= 0,1 . 2 = 0,2 (g)
Câu 23 :
Cho 6,5 gam Zn phản ứng với axit clohiđric (HCl) thấy có khí bay lên với thể tích là
Đáp án : A Phương pháp giải :
+) Tính số mol H2 theo PTHH: Zn + 2HCl → ZnCl2 + H2 Lời giải chi tiết :
Số mol Zn là: ${{n}_{Zn}}=\frac{6,5}{65}=0,1\,mol$ PTHH: Zn + 2HCl → ZnCl2 + H2 Tỉ lệ PT: 1mol 1mol P/ứng: 0,1mol → 0,1mol => thể tích khí bay lên là: ${{V}_{{{H}_{2}}}}=0,1.22,4=2,24$ lít
Câu 24 :
Cho mẩu Na vào cốc nước dư thấy có 4,48 lít khí bay lên ở đktc. Tính khối lượng Na phản ứng
Đáp án : A Phương pháp giải :
+) Tính số mol khí H2 +) Viết PTHH, tính số mol Na theo số mol H2
Lời giải chi tiết :
Khí bay lên là H2 Số mol khí H2 là: ${{n}_{{{H}_{2}}}}=\frac{4,48}{22,4}=0,2\,mol$ PTHH: 2Na + 2H2O → 2NaOH + H2 Tỉ lệ PT cứ thu được 1mol H2 thì cần dùng 2 mol Na P/ứng: thu được 0,2mol H2 thì cần dùng: 0,2.2=0,4 mol Na => Khối lượng Na phản ứng là: mNa = 0,4.23 = 9,2 gam
Câu 25 :
Cho 0,1 mol NaOH tác dụng với 0,2 mol HCl, sản phẩm sinh ra sau phản ứng là muối NaCl và nước. Khối lượng muối NaCl thu được là
Đáp án : B Phương pháp giải :
+) Viết PTHH: NaOH + HCl → NaCl + H2O và xét tỉ lệ dư thừa +) tính số mol NaCl theo số mol chát hết => khối lượng
Lời giải chi tiết :
PTHH: NaOH + HCl → NaCl + H2O Xét tỉ lệ: $\frac{{{n}_{NaOH}}}{1}=0,1<\frac{{{n}_{HCl}}}{1}=0,2$ => HCl dư, NaOH phản ứng hết => tính số mol NaCl theo NaOH PTHH: NaOH + HCl → NaCl + H2O Tỉ lệ PT: 1mol 1mol 1mol P/ứng: 0,1mol → 0,1mol => Khối lượng muối NaCl thu được là: mNaCl = 0,1.58,5 = 5,85 gam
|


















